目录
血脂 心血管风险
**血脂与心血管风险**
2023 年 12 月 15 日
本文将讨论血脂,例如 LDL 胆固醇、HDL 胆固醇和甘油三酯,以及如何影响患心血管疾病(例如心脏病或中风)的风险。出于某种原因,这已成为一个热门话题,我从许多人那里听到最多的一件事是,对这个问题完全感到困惑,因为有太多的声音,其中一些人声称 LDL 胆固醇是心血管疾病的真正原因,应该服用他汀类药物,而另一些人则声称这都是大型制药公司的阴谋诡计,LDL 胆固醇对心血管疾病的影响可以忽略不计。
我写这篇文章的目的是让这个领域更加清晰,不仅仅是通过增加另一种声音,而是通过手把手地指导,回顾分析所有不同的证据,以及争论双方的各种声明。我的目标是,读完本文将更清楚地了解这个重要主题的科学原理,即血脂与心血管疾病的关系、LDL-胆固醇等脂质相对于其他风险因素的重要性、需要进行哪些化验检测以及如何解释这些检测结果。
快速免责声明:我与制药或补剂行业没有任何关系,与本文内容没有任何经济利益。我只是分享我看到和理解的数据。与往常一样,我准备了另外一篇博客文章,更详细地讨论了本文中涉及的一些问题,并提供了所有科学参考文献。与往常一样,链接位于文章下方描述框中。
**动脉粥样硬化性心血管疾病的基础知识**
首先要明确一点,心血管疾病有很多种。本文感兴趣的是动脉粥样硬化性心血管疾病,简称 ASCVD。ASCVD 是指动脉壁上斑块的逐渐积累,随着时间的推移,斑块不断增大,动脉内部收缩,导致血液无法自由流动。下图所示的这一过程,称之为动脉粥样硬化。在晚期阶段,斑块会变得不稳定,发生破裂,此时动脉将完全闭合。如果这是一条为心肌提供营养和氧气的重要动脉,那么就会导致心脏病发作。如果这是一条为大脑供血的动脉,那么就会导致中风。
希望您从本文学到的第一件事是,动脉粥样硬化显然是一种多因素疾病,有许多独立的风险因素,每个因素都会促进其发展。这些因素包括年龄、性别和种族,以及吸烟、高血压、糖尿病和肾病。LDL-胆固醇浓度也被认为是这些已确定的风险因素之一,这似乎是合理的,因为动脉壁上的斑块实际上主要由胆固醇组成。还应考虑一些其他血脂指标,例如 HDL-胆固醇、甘油三酯和一种称为 Lp(a) 的 LDL 样颗粒。
因此,ASCVD 是一种多因素疾病,暴露于多个或所有风险因素的人群动脉粥样硬化发生进展最快。然而,每个因素仍然是一个独立的风险因素,这意味着即使只有一个因素独立于所有其他因素而升高,也会增加 ASCVD 风险。在本文中研究的一个独立风险因素是血脂状况,特别关注空腹 LDL 胆固醇浓度。
**血脂和脂蛋白的基础知识**
这部分内容会有点技术性,因为了解血液中不同脂蛋白的类别对于理解文章后面的细微差别是必要的。
甘油三酯和胆固醇等脂肪不溶于血液,因此需要包装以便运输。血液中的脂肪运输蛋白称为脂蛋白。在空腹状态下,血液中有多种脂蛋白。您可能听说过两种脂蛋白,即低密度脂蛋白(LDL)和高密度脂蛋白(HDL)。现在我想提一下另外两种脂蛋白:极低密度脂蛋白(VLDL)和中密度脂蛋白(IDL)。
这些脂蛋白都含有脂质,如甘油三酯和胆固醇,也含有蛋白质。不同的脂蛋白所携带的脂质和蛋白质的类型以及脂质与蛋白质的相对比例各不相同。脂质和蛋白质的相对比例会影响其密度。这是因为脂质的密度小于1 g/mL,而蛋白质的密度大于1.3 g/mL。因此,主要由脂质组成的脂蛋白的密度接近1,而含有相对较多蛋白质的脂蛋白的密度约为1.2。
密度最低的脂蛋白是 VLDL,然后是 IDL、LDL,密度最高的是 HDL。这些脂蛋白不仅密度不同,大小也不同,VLDL 最大,HDL 最小。如上图所示,每种脂蛋白类别的密度和大小实际上都存在一定范围,因此,假设所有 LDL 颗粒完全相同并不准确。相反,实际情况是,这些脂蛋白类别的密度和大小分布在整个范围内。这一点在后面会变得很重要。
VLDL 颗粒由肝脏分泌,也含有胆固醇,但甘油三酯含量特别丰富。VLDL 颗粒随后会脱落甘油三酯(主要存在于脂肪组织中),在此过程中会收缩,脂蛋白颗粒中蛋白质的比例越来越大,请记住,蛋白质比脂质密度大。意味着颗粒的密度会增加。下面动画可查看此过程的说明。
因此,如下图所示,肝脏分泌的 VLDL 颗粒逐渐变成 IDL,然后变成 LDL。颗粒失去甘油三酯并收缩,密度增加。在此过程中,颗粒内蛋白质和胆固醇的相对比例增加。肝脏还可以直接将 IDL 和 LDL 颗粒释放到血液中。因此,VLDL、IDL 和 LDL 都来自肝脏,在某种程度上是相互关联的。事实上可以说它们是同一种颗粒,只是处于生命周期的不同阶段。
 VLDL、IDL 和 LDL 均由肝脏产生,都是同一种脂蛋白颗粒:大部分由肝脏产生,形成富含甘油三酯的 VLDL,这些颗粒会脱落脂肪组织中的甘油三酯并收缩,从而变成 IDL,然后变成 LDL
VLDL、IDL 和 LDL 均由肝脏产生,都是同一种脂蛋白颗粒:大部分由肝脏产生,形成富含甘油三酯的 VLDL,这些颗粒会脱落脂肪组织中的甘油三酯并收缩,从而变成 IDL,然后变成 LDL
相比之下,高密度脂蛋白HDL颗粒则不同,颗粒非常小,密度非常高,富含蛋白质。虽然高密度脂蛋白中的关键蛋白质可以由肝脏制造,也可以由肠道制造,但在血液中循环时会吸收大部分脂质物质,例如胆固醇。完整的脂蛋白颗粒实际上是在高密度脂蛋白颗粒在血液中循环时形成的。
如果进行 LDL 胆固醇检测,检测测量的是所有 LDL 颗粒中运输的胆固醇含量。同样,HDL 胆固醇是所有 HDL 颗粒中运输的胆固醇。两种情况下的胆固醇是同一种分子;只是运输载体不同。而且,正如稍后将讨论的那样,哪种运输载体携带血液中的胆固醇对 ASCVD 风险确实很重要。
这些脂蛋白类别之间还有一个主要区别,即携带的主要蛋白质的类型(见上图)。这一点很重要,因为这会影响这些脂蛋白的功能、从血液中的清除,以及如何影响 ASCVD 风险。VLDL、IDL 和 LDL 中的关键脂蛋白称为Apo B 载脂蛋白 B,HDL 中的关键脂蛋白称为Apo A 载脂蛋白 A。稍后会讨论为什么这很重要。
现在脂蛋白的基本知识已经更清楚了。接下来了解一下这些脂蛋白与 ASCVD 之间的关系。
**LDL 颗粒会导致 ASCVD 吗?**
LDL 颗粒会导致 ASCVD 吗?至少,这是这篇科学论文所提出的主张。这不是一篇普通的论文:这是一份立场声明,其作者是这个时代最著名的脂质研究人员。那么他们为什么会得出这个异常有力的结论呢?LDL 颗粒会导致 ASCVD。除非有非常有力的证据,否则科学家通常不会使用这样的强烈因果关系语言。让我们看看他们提出的证据,一起思考一下。
他们提出的第一个证据是,天生LDL 胆固醇浓度极高的人患 ASCVD 的风险往往会大大增加。文献中确实有报道称,LDL 胆固醇浓度大幅升高至 400、500、600 mg/dL 以上的幼儿在进入青春期之前会心脏病发作。这些情况很少见,但表明,尽管 ASCVD 是一种多因素疾病,但如果这一风险因素 LDL 胆固醇完全失控,其本身就会在很小的时候导致严重的 ASCVD 及其临床表现,而且没有任何证据表明存在其他促成风险因素,如吸烟、高血压或糖尿病。我有一个叔叔有遗传缺陷,导致他的 LDL 胆固醇水平非常高。他在 29 岁时第一次心脏病发作,他家里的几乎每个人都在 60 岁之前死于 ASCVD。
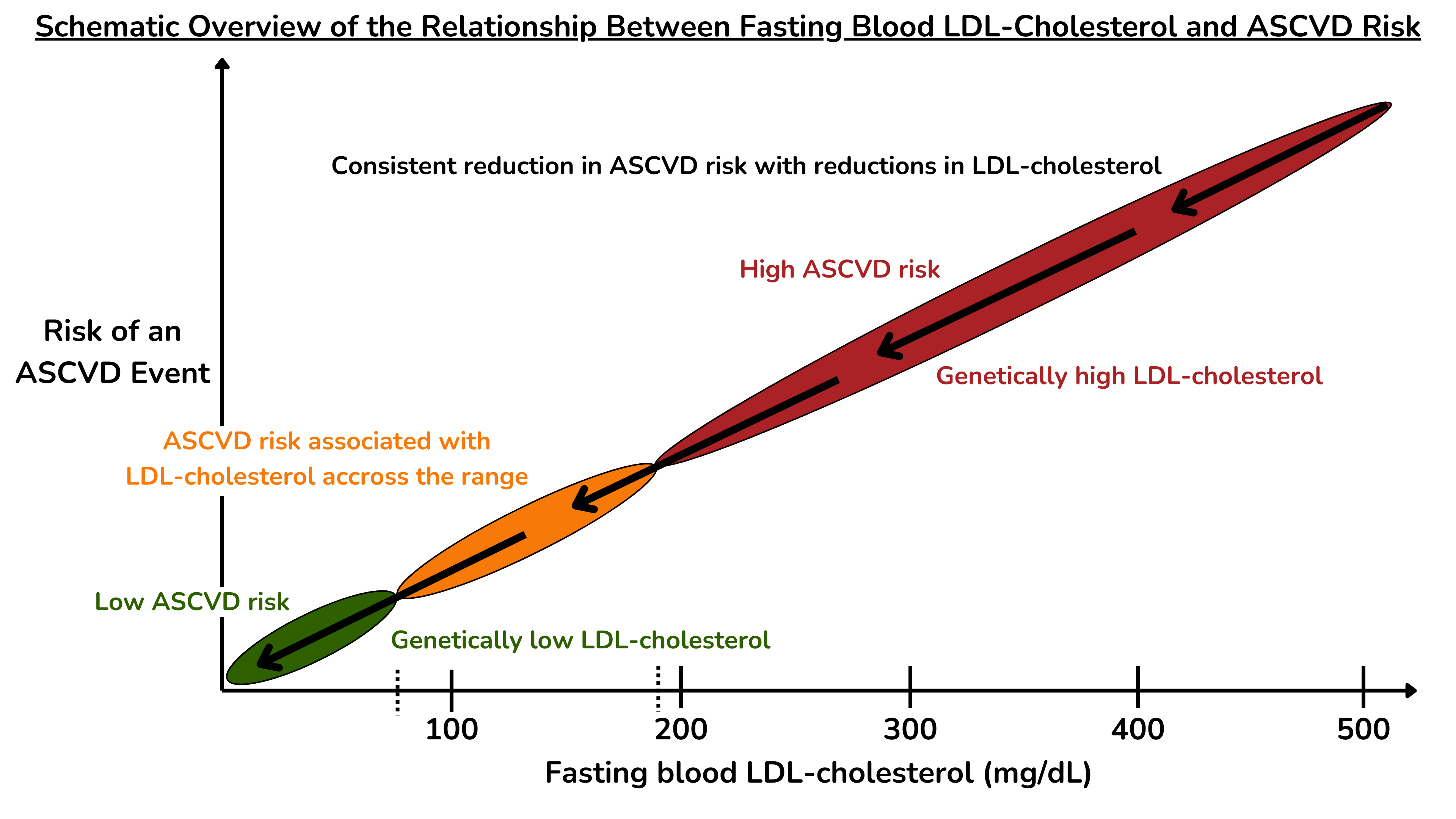 基于遗传、观察性和干预研究,示意图概述了血清 LDL 胆固醇水平与 ASCVD 风险之间的关系。
基于遗传、观察性和干预研究,示意图概述了血清 LDL 胆固醇水平与 ASCVD 风险之间的关系。
另一方面,有些人的 LDL 胆固醇水平从基因上来说非常低。他们中的大多数人体内有一种名为 PCSK9 的蛋白质,该蛋白质的功能丧失了。无论他们吃什么,有些人的 LDL 胆固醇浓度在高龄期间一直保持在 20、30 或 40 mg/dL。他们患心脏病的风险是多少?是的,确实非常低。
现在,大多数有据可查的遗传性极高 LDL 胆固醇浓度病例的 LDL 胆固醇水平为 190 mg/dL以上,在许多情况下甚至更高。而那些遗传性极低 LDL 胆固醇浓度的病例的 LDL 胆固醇水平通常低于 70 mg/dL。那么大多数没有重大基因突变的人处于的 70 到 190 mg/dL 之间的中间范围呢?同样如此:在广泛的研究中,即使在这个范围内,较高的 LDL 胆固醇浓度也与较高的 ASCVD 风险相关。
LDL 胆固醇与 ASCVD 风险相关,但相关性并不等同于因果性,所以接下来看看通过实验降低 LDL 胆固醇的临床试验。已发表有多项试验,总共有超过 200 万参与者,其目标是降低 LDL 胆固醇。这些试验包括几类降脂药物的试验,包括他汀类药物、依折麦布、贝伐单抗酸和 PCSK9 抑制剂。但也有干预数据,在这些干预措施中,无需使用任何药物,以机械方式从血液中去除 LDL 胆固醇,这一过程称为 LDL 分离术,类似于透析,血液通过机器,然后从血液中去除 LDL 颗粒。无论如何降低 LDL 胆固醇,这些试验都表明ASCVD 风险持续降低,并且斑块体积也减少。而且,干预措施降低 LDL 胆固醇的力度越大,ASCVD 风险通常就越低。
这里特别有趣的一点是,模仿某些降脂药物效果的基因变异似乎对 LDL 胆固醇和 ASCVD 风险的影响与药物相同。例如,他汀类药物抑制一种名为 HMG-CoA 还原酶的酶,这种酶是胆固醇合成的关键酶。服用他汀类药物的人的 HMG-CoA 还原酶活性较低,因此 LDL 胆固醇水平较低,ASCVD 风险较低。现在有趣的部分来了。如果在普通人群中发现具有不同基因的人,要么具有非常活跃的 HMG-CoA 还原酶,要么具有受抑制的版本,那会怎么样?那些具有受基因抑制、活性较低的 HMG-CoA 还原酶的人往往 LDL 胆固醇水平较低,就像服用他汀类药物的人一样,因此,他们患 ASCVD 的风险也较低。 PCSK9 的情况也完全一样,PCSK9 抑制剂类药物针对的是该种酶。换句话说,从基因上降低这些酶的功能对 LDL 胆固醇水平和 ASCVD 风险的影响与从药理上抑制的影响相似。
除了来自大规模观察性、遗传性和干预性研究的证据外,现在还有确凿的证据表明LDL 颗粒和其他含载脂蛋白 B 在动脉粥样硬化的病因中起着至关重要的作用。本质上,正是这些含载脂蛋白 B 的颗粒滞留在动脉内皮层下的空间中,引发了第一个动脉粥样硬化病灶的形成。与来自观察性、遗传性和干预性研究的证据一致,较高浓度的 LDL 颗粒和其他含载脂蛋白 B 的脂蛋白似乎会加速这一过程。同样与其他 ASCVD 风险因素的证据一致,毫无疑问,其他暴露也会大大增加这一过程,特别是糖尿病、高血压和吸烟。
总之,我同意上面立场声明文件作者的观点,即现有数据强烈表明 LDL 胆固醇浓度升高是 ASCVD 的主要独立风险因素,并且可能是因果关系。我建议考虑这些证据,如果仍然怀疑 LDL 胆固醇在 ASCVD 中的作用,建议阅读一些原始文献。
在科学领域,很少能获得如此一致的证据。我们应该始终对新数据持开放态度,可能还会了解到一些有关 LDL 胆固醇与 ASCVD 风险之间关系的新信息,将在后面讨论,但目前,现有的证据非常有力且一致。
**LDL 胆固醇是否是评估 ASCVD 风险的最佳血脂指标?**
因此这就引出了一个问题:LDL 胆固醇是否是评估 ASCVD 风险的最佳血脂指标。
简短的回答是“否”。近年来了解到,不仅 LDL 颗粒会致动脉粥样硬化,VLDL 和 IDL 颗粒也会致动脉粥样硬化。而且现在也更好地了解到,预测 ASCVD 风险的最佳血脂指标不是这些脂蛋白携带的胆固醇量,而是血液中这些致动脉粥样硬化颗粒的数量。
现在能测量血液中这些颗粒的数量吗?能。还记得 VLDL、IDL 和 LDL 都携带一种称为载脂蛋白 B 的蛋白质吗?事实上,这些脂蛋白颗粒中的每一个都携带一个载脂蛋白 B 分子。因此,可以测量血液中载脂蛋白 B 的浓度,该测量值与血液中动脉粥样硬化颗粒的总数直接相关。因此,预防心脏病专家和脂质学家目前的共识是,血浆载脂蛋白 B 是脂质相关 ASCVD 风险的最佳衡量标准。
如果无法测量载脂蛋白 B,那么第二好的选择就是非高密度脂蛋白胆固醇。非高密度脂蛋白胆固醇等于总胆固醇减去高密度脂蛋白胆固醇,因此可以通过标准血脂检测结果自行计算。非高密度脂蛋白胆固醇不是动脉粥样硬化脂蛋白颗粒数的直接测量值,而是胆固醇含量的测量值,胆固醇含量与颗粒数密切相关。因此,非高密度脂蛋白胆固醇是第二好的测量值。
那么 LDL 胆固醇就没用了吗?不是的,因为LDL与载脂蛋白 B 和非 HDL 胆固醇相关。然而,LDL 胆固醇有一个小小的缺点:不测量与 VLDL 和 IDL 颗粒相关的任何物质。而且,正如我所提到的,这些颗粒和 LDL 一样,也是动脉粥样硬化颗粒。
总结一下这部分:理想情况下,测量空腹血液中的载脂蛋白 B 浓度,或者作为第二和第三选择,分别测量非 HDL 胆固醇或 LDL 胆固醇。
现在,还有另一种经常被遗忘的脂蛋白:脂蛋白 (a),或 Lp(a)(“Lp little a”)。Lp(a) 是另一种类似于 LDL 的脂蛋白,不仅有一个载脂蛋白 B 分子,还有一种称为载脂蛋白 (a) 的额外蛋白质。
 然而,除了 apo B 之外,Lp(a)的外表面还携带一种额外的蛋白质:apo(a)。
然而,除了 apo B 之外,Lp(a)的外表面还携带一种额外的蛋白质:apo(a)。
现在这很令人困惑,这值得了解和充分理解。LDL 颗粒上的主要蛋白质是 apo B,HDL 颗粒上的主要蛋白质是 apo A,大写 A。现在还有一种你可能从未听说过的颗粒,叫做 Lp(a),既有 apo B,又有另一种叫做 apo(a) 的蛋白质,但没有大写 A,很抱歉这些东西的命名这么复杂,但与我无关。一旦你理解了,也就不那么复杂了。所以,再说一次,VLDL、IDL 和 LDL 颗粒都有一个共同的主要蛋白质,那就是 apo B。HDL 颗粒都有 apo A,大写 A。然后是 Lp(a),在很多方面都像 LDL,包括有 apo B,但其外表面上还有一种叫做 apo(a) 的额外蛋白质。这有点超出通常考虑和谈论的脂蛋白的范围,因为它比大多数 LDL 颗粒大,直径约为 25 纳米。但由于它比 LDL 颗粒多了一种蛋白质,而且蛋白质比脂质密度大,所以其密度往往比 LDL 略大。介于 LDL 颗粒和 HDL 颗粒之间(见下图)。
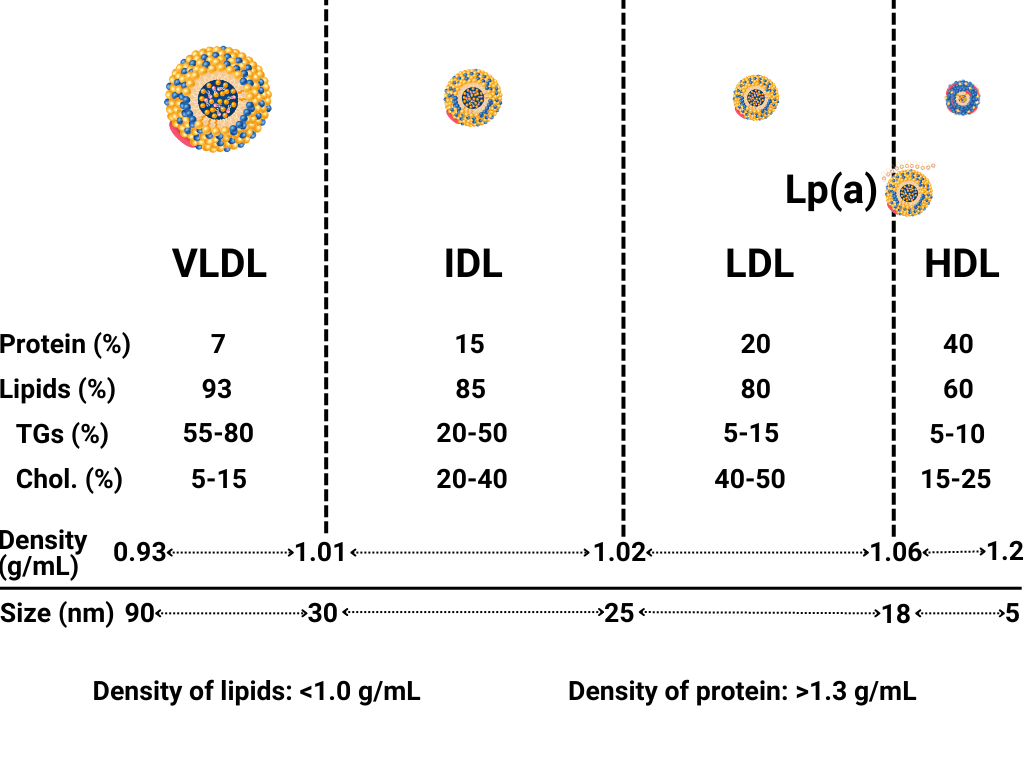 Lp(a) 的平均尺寸为 25 纳米,也就是说,比大多数 LDL 颗粒都大。然而,其密度也更大,与较大的 HDL 颗粒的密度相似。
Lp(a) 的平均尺寸为 25 纳米,也就是说,比大多数 LDL 颗粒都大。然而,其密度也更大,与较大的 HDL 颗粒的密度相似。
那为什么这很重要,值得在这提及?因为Lp(a) 被认为是 ASCVD 的更大风险因素,其原因多种多样,超出了本文的讨论范围。可以说,需要知道身体的 Lp(a) 水平是低还是高。
现在,如果测量载脂蛋白 B 浓度,这确实包括 Lp(a) 颗粒,因为它们也含有一个载脂蛋白 B 分子。此外,如果测量非高密度脂蛋白胆固醇,这些测量的确会测量所有非高密度脂蛋白颗粒中的胆固醇含量,包括 Lp(a)。测量低密度脂蛋白胆固醇的最常用方法实际上不是化验,而是一种计算,实际上是不仅估计 LDL 颗粒的胆固醇浓度,而且估计 LDL 颗粒加上 Lp(a) 颗粒的胆固醇浓度。如果想知道为什么会这样,大多数情况下,LDL 胆固醇并不是实际测量的,而是使用所谓的 Friedewald 公式计算的:
LDL 胆固醇(计算值)= 总胆固醇 - HDL 胆固醇 - (甘油三酯 / 5)。
通常,高密度脂蛋白胆固醇的测量方法是,从血液中去除含有载脂蛋白 A 的脂蛋白,然后测量其中的胆固醇浓度。甘油三酯之所以包含在此公式中,是因为甘油三酯浓度除以 5 平均可以很好地近似 VLDL 和 IDL 颗粒中的胆固醇含量。剩下的作为计算出的 LDL 胆固醇浓度的是非 HDL、VLDL 或 IDL 脂蛋白颗粒中的胆固醇含量,这些是 LDL 和 Lp(a)。
那么为什么要用这些复杂的东西来表达?因为尽管 Lp(a) 包含在载脂蛋白 B、非高密度脂蛋白胆固醇和低密度脂蛋白胆固醇中,但比其他致动脉粥样硬化脂蛋白更容易致动脉粥样硬化,因此了解其浓度可以提高预测 ASCVD 事件的能力。关于 Lp(a)的有趣之处在于,大多数人的血浆浓度都很低,低浓度定义为低于 30 mg/dL。然而,在大约 20% 的人中,Lp(a)可能会升高,主要是由于遗传原因。我们认为 Lp(a)浓度为 30 至 50 mg/dL 为中度升高,浓度为 50 mg/dL 或更高为大幅升高。由于 Lp(a) 在很大程度上由基因决定,因此一生中只需测量一次 Lp(a) 就足够了,然后利用这些信息来衡量总体风险,如果 Lp(a) 浓度超过 30 mg/dL 尤其是 50 mg/dL,则要更积极地解决的其他 ASCVD 风险因素。顺便说一句,这里的转换并不简单,但如果检测结果提供的 Lp(a) 浓度以 nmol/L 为单位,可以将其除以 2.25 以获得以 mg/dL 为单位的浓度估算值。
总而言之,要考虑的一个关键指标是载脂蛋白 B 或非高密度脂蛋白胆固醇或低密度脂蛋白胆固醇。然后在一生中测量一次 Lp(a),以确定可能需要多大程度地关注其他 ASCVD 风险因素。
我想谈谈另外两个 ASCVD 风险因素:高密度脂蛋白胆固醇和甘油三酯。
首先是高密度脂蛋白胆固醇。这是高密度脂蛋白颗粒上携带的胆固醇量,一般来说,此胆固醇水平越高,ASCVD 风险越低。然而,高密度脂蛋白颗粒和 ASCVD 之间的关系很复杂,全面讨论超出了本文的范围。简而言之,目前的理解是,高密度脂蛋白确实具有有效的抗动脉粥样硬化功能,但这些功能与其携带胆固醇的关系较小,而与其相关的 50 多种蛋白质的组成和功能的关系更大。此外,到目前为止,尚未发现提高高密度脂蛋白胆固醇会降低 ASCVD 风险。不过,可以说,高密度脂蛋白胆固醇仍然用于 ASCVD 风险预测模型,并且还有助于检测胰岛素抵抗综合征的出现,正如上一篇文章中所讨论的那样。
HDL 胆固醇的替代测量指标是载脂蛋白 A(最常见的是载脂蛋白 A1),有时也会查看比率,例如总胆固醇与 HDL 胆固醇的比率、LDL 胆固醇与 HDL 胆固醇的比率以及载脂蛋白 B 与载脂蛋白 A 的比率。这些一般来说是不必要的复杂。注意载脂蛋白 B、非 HDL 胆固醇或 LDL 胆固醇。考虑 Lp(a),然后考虑 HDL 胆固醇或载脂蛋白 A。这是三个关键的血脂相关 ASCVD 风险因素。
评估 ASCVD 风险的关键血脂指标
那么甘油三酯呢?一般来说,甘油三酯升高与 ASCVD 风险增加有关。但是,一旦考虑到所有其他风险因素,无论是否有高甘油三酯通常都不会增加那么多,因此风险预测模型中通常不会考虑甘油三酯。原因是空腹甘油三酯水平升高的人通常 HDL 胆固醇水平也较低,更容易患高血压和 2 型糖尿病。一旦这些因素被纳入风险预测模型,添加甘油三酯通常不会提高模型预测 ASCVD 事件风险的能力。这就是为什么我认为甘油三酯主要用作代谢健康的衡量标准,正如上一篇关于胰岛素抵抗综合征的文章中所解释的那样。
到目前为止讨论的内容可能听起来很有说服力,但可能仍然会困惑,因为有相互矛盾的信息。
**回应那些认为 LDL 胆固醇不是 ASCVD 风险因素的常见说法**
本节将讨论几个质疑 LDL 胆固醇在 ASCVD 中的作用的具体说法。具体将讨论:
- 许多心脏病发作的人的 LDL 胆固醇水平正常,因此 LDL 胆固醇不能成为 ASCVD 的原因;
- 降低 LDL 胆固醇只能最低程度地降低绝对 ASCVD 风险,这表明 LDL 胆固醇并不是那么重要;
- 只有小而密的 LDL 才是有害的;
- 其他风险因素,如胰岛素抵抗或代谢健康,比 LDL 胆固醇更重要,因此可以安全地忽略 LDL 胆固醇;
- 低碳水饮食或生酮饮食导致的LDL 胆固醇升高不会导致动脉粥样硬化;
- 胆固醇是无害的,因为是人体产生的天然物质,而且是人体许多重要功能所必需的。
所有这些都是 YouTube 视频中常见的话题,这些视频的观看次数达到数百万次,通常由拥有医学博士或哲学博士学位的人提出,所以我认为在这解决这些问题很重要,因为这些是很多混乱的根源。
**说法 1:许多心脏病发作的人的 LDL 胆固醇水平正常**
经常听到的第一个说法是,许多心脏病发作的人的 LDL 胆固醇水平正常,因此 LDL 胆固醇不能成为 ASCVD 的原因。
毫无疑问,许多人即使 LDL 胆固醇浓度从未特别高,也会患心脏病。然而,在心脏病患者中,也有许多人没有糖尿病、不吸烟、没有慢性肾病,但没有人质疑糖尿病、吸烟和肾病是 ASCVD 的主要独立风险因素。同样,重要的是所有风险因素的累积暴露。
此外,应该考虑到,即使是传统上认为“正常”的 LDL 胆固醇浓度,例如 90-110 mg/dL (2.4-2.9 mmol/L),仍然与动脉粥样硬化的进展有关,如果与其他风险因素相结合,肯定会导致临床 ASCVD 事件。与此同时,对于 LDL 胆固醇浓度极低(50 mg/dL (1.3 mmol/L)以下)的个体来说,ASCVD 事件极为罕见。因此,这种说法部分源于对“正常” LDL 胆固醇水平的错误定义,部分源于没有考虑其他 ASCVD 风险因素的独立贡献。
**说法 2:降低 LDL 胆固醇只能最低程度地降低 ASCVD 绝对风险**
第二种说法是,降低 LDL 胆固醇只能最低程度地降低绝对 ASCVD 风险,这表明 LDL 胆固醇并不是那么重要。
这一说法与一个重要的统计概念有关,即相对风险降低和绝对风险降低之间的差异。假设要对 LDL 胆固醇水平升高的人进行试验,随机分为降脂药物组或安慰剂组。4 年来,一个典型的发现可能是安慰剂组中 4% 的人发生心血管事件,例如心脏病发作或中风,而治疗组中只有 3% 的人发生心血管事件。在这个例子中,与安慰剂组相比,治疗组的相对风险降低了 25%。这就是经常报告的数字。但是,绝对风险只降低了 1%,对吗?从 4% 到 3%,批评者经常评论说,制药公司在报告其试验数据时夸大了他们非常温和的发现,报告的是相对风险降低而不是绝对风险降低。
那么怎么看这?这是作弊吗?或者觉得从相对的角度考虑风险降低有意义吗?需要澄清的是,绝对风险降低非常小的说法完全正确,数据中也清楚地表明了这一点,因此无需争论。
但是,我完全不同意这里的批评者。而且坦率地说,我实际上认为他们的论点是没有经过深思熟虑的。为什么会这样?首先,很显然,如果即使在安慰剂组中,也只有 4% 的人发生心血管事件,那么绝对风险降低幅度就会很小。但是,更重要的一点是,大多数人不仅对在未来 4 年内保持健康感兴趣。相反,大多数人可能都希望在未来 10、15、20 甚至 25 年内尽量降低心脏病发作或中风的风险,那么,如果将这些推断到 20 年会怎样?现在需要清楚,我们无法知道会发生什么,我们只能猜测。但考虑到 4 年后观察到的差异,我敢说,最好的估计是风险的绝对差异将远远大于 4 年后观察到的 1%。
短期内较小的绝对风险降低预计会在长期内逐渐增大为较大的绝对风险降低。
在这方面,我想强调一点:思考 LDL 胆固醇或载脂蛋白 B 与 ASCVD 风险之间关系的正确方法是将浓度乘以暴露时间。因此,不应该将当前的 LDL 胆固醇水平视为风险因素,而应该将一生中 LDL 胆固醇浓度下的面积视为风险因素。也许就像下图中 60 岁老人的情况一样。时间在 x 轴上,而这 60 年内的 LDL 胆固醇水平在 y 轴上。因此,如果某人一生的 LDL 胆固醇浓度都很高,而且越来越高,并在 60 岁时开始服用降脂药物,那么发生心血管事件的风险不仅取决于现在降低的 LDL 胆固醇水平,而取决于一生中所有 LDL 胆固醇水平的总和。最初,接受治疗的人与未接受治疗的人在总体暴露方面差异很小。看看4 年后,在 LDL 胆固醇曲线下方用黄色标记的区域将成为开始降脂治疗的人与未开始降脂治疗的人之间的唯一差异。一生中 LDL 胆固醇的总体暴露差异很小。所以,可以在几年内检测到心血管事件风险的差异,这一事实充分说明了 LDL 胆固醇在 ASCVD 中的重要性。
对于包括 LDL 胆固醇在内的每种风险因素,最重要的暴露量是累积终生暴露量,可通过曲线下面积(此处浅绿色阴影)来衡量。重要的是要考虑到任何降脂疗法对累积暴露量的影响在短期内都很小。绿色:60 岁时开始接受降脂疗法的人。红色:未开始接受降脂疗法的人。
最后一点是,通过降低 LDL 胆固醇,只能解决这种多因素疾病中的众多风险因素之一。在短期内,治疗高血压或糖尿病或戒烟也能带来类似的、相当小的好处。我强烈地感觉到,如果解决每个风险因素,并将我暴露程度降至最低,那么短期内几个小影响的总和有望在较长时间内产生巨大的相对和绝对利益,而这可能正是大多数人感兴趣的。下图以示意图的形式说明了这一概念。请注意,这些图表并非基于实际数据;但是,短期影响在方向上与已发表的试验一致。
当解决多个风险因素时,ASCVD 风险的短期绝对降低可以累积起来,并在长期内导致绝对风险大幅降低。注意:图表的方向正确,但不是基于实际数据的。
综合起来,考虑到终生暴露很重要,而且有许多风险因素会导致 ASCVD,根本不能指望单单解决一个风险因素就能在短期内带来很大的绝对效益。但是,如果将几个 ASCVD 风险因素的几个看似很小的短期效益叠加起来,从长远来看,风险将大大降低。
**说法3:只有小而密的LDL颗粒才会导致动脉粥样硬化**
第三个说法是,只有小而致密的 LDL 颗粒才会导致动脉粥样硬化,而大而有浮力或蓬松的 LDL 颗粒则无害。这到底是怎么回事?
还记得在本文开头讨论脂蛋白基础知识时说过的吗?VLDL、IDL 和 LDL 在密度和大小方面都有很大差异。这意味着有些 LDL 颗粒比其他颗粒更小、更致密。我们称这些颗粒为小而致密的 LDL 颗粒,而那些颗粒另一端的颗粒则为大而有浮力的或“蓬松的”LDL 颗粒。一种普遍的说法是,只有当我们拥有许多这种小而致密的 LDL 颗粒时,ASCVD 的风险才会增加,而大而蓬松的 LDL 颗粒则无害。
首先要解决的问题是,小而密的 LDL 颗粒是否真的比大而松散的 LDL 颗粒更容易导致动脉粥样硬化。是的,有相当多的证据表明,这些小而密的 LDL 颗粒具有某些特性,使其更容易导致动脉粥样硬化。例如,它们似乎富含除载脂蛋白 B 以外的某些蛋白质,这可能使其更容易导致动脉粥样硬化。它们更容易受到氧化损伤和糖化;糖化是指糖分子附着在颗粒内的蛋白质上。与较大的载脂蛋白 B 颗粒相比,它们可能更容易进入内皮下空间。而且它们在血液循环中停留的时间也比大而松散的 LDL 颗粒更长,因为它们对 LDL 受体的结合亲和力低于大而浮力强的 LDL 颗粒。还要记住,小而密的 LDL 更致密,因为比大而松散的 LDL 含有更多的蛋白质和更少的胆固醇。因为 LDL 颗粒中的主要蛋白质是载脂蛋白 B,这意味着,如果拥有更多小而密的 LDL 颗粒,那么在相同的 LDL 胆固醇水平下,血液中的载脂蛋白 B 浓度就会更高。
因此,体积小、密度高的 LDL 颗粒比体积大、松散的 LDL 颗粒多,可能与 ASCVD 风险增加有关。但这是否意味着体积大、松散的 LDL 颗粒无害呢?
首先,没有人只有小而密的 LDL 颗粒,也没有人只有大而浮力强的 LDL 颗粒。要理解这一点,首先要弄清楚如何确定拥有哪种 LDL 颗粒。有许多不同的方法可以确定这一点,实验室使用的一种方法是分别测量每种 LDL 类型的胆固醇含量。因此,不仅会将 VLDL 与 IDL、LDL 与 HDL 分开,还会在每个类别中再次分开。因此,对于 LDL,会分离出 12 种不同类型的 LDL,然后测量每种类型的胆固醇含量(见下图)。
来看看我自己的一项临床试验中的两名参与者。这两名参与者的总体 LDL 胆固醇水平完全相同,但如果分别测量每种不同类型的 LDL 中的胆固醇含量,会发现蓝线标记的人大部分胆固醇都存在于较大且蓬松的 LDL 颗粒中,或者属于中等类型,而小而密的 LDL 颗粒中的胆固醇含量非常少。另一方面,红线标记的人大部分胆固醇都存在于小而密的 LDL 颗粒中。如果只量化小而密的 LDL 颗粒中的胆固醇含量,蓝线的胆固醇含量为 60 mg/dL,而红线的胆固醇含量为 88 mg/dL。同样,尽管两人的 LDL 胆固醇浓度完全相同。在不了解这些人其他情况的情况下,会假设红线的小而密 LDL 含量更多,患 ASCVD 的风险更高。但要记住的一点是,即使在这些相对极端的情况下,两个人体内也都混合有小而密的 LDL 颗粒和大而蓬松的 LDL 颗粒。
图中显示了整个密度范围内 VLDL、IDL、LDL 和 HDL 颗粒中的胆固醇含量,这使我们能够识别出 LDL 胆固醇主要存在于小而致密的 LDL 颗粒中的个体,如红线所示。然而,蓝线所代表的人在其小而致密的 LDL 颗粒中携带的胆固醇很少。
通过将图中的红蓝线与绿线进行对比,可以得出另一个重要结论。绿线代表的人整体 LDL 颗粒中的胆固醇要少得多。换句话说, LDL 胆固醇水平较低,实际上低了 65%。小而密的 LDL 中的胆固醇含量为 26 毫克/分升,比红蓝线低得多。所以在这里了解到,如果 LDL 胆固醇水平高,即使其中大多数颗粒既不小而密,比如蓝线,与整体 LDL 胆固醇水平低的人相比,小而密 LDL 颗粒的绝对浓度仍然可能相对较高。所以,第二点是,决定小而密 LDL 颗粒数量的最大因素之一是总 LDL 胆固醇浓度。
第三,还要明确的是,认为大而蓬松的 LDL 颗粒无害的想法与文献不一致。人们普遍认为,所有载脂蛋白 B 颗粒在某种程度上都是导致动脉粥样硬化的;只是小而密的颗粒可能更容易致动脉粥样硬化。在预测谁会患上 ASCVD 的统计模型中,大多数研究中的总 LDL 胆固醇仍然与 ASCVD 风险密切相关,即使在模型中添加了小而密 LDL 的衡量标准。换句话说,考虑小而密 LDL 颗粒的数量,或小而密 LDL 颗粒中的胆固醇含量,可能会提高预测 ASCVD 事件的能力,但这只是对 LDL 胆固醇预测价值的补充,而不是替代。对于载脂蛋白 B 来说更是如此,因为总载脂蛋白 B 往往与小而密 LDL 颗粒的数量相关。
第四,转变为小而密 LDL 增多主要见于胰岛素抵抗和潜在的葡萄糖不耐受人群、内脏和肝脏脂肪过多、甘油三酯升高和 HDL 胆固醇降低、患有低度慢性炎症和高血压的人群。换句话说,拥有小而密的 LDL是在上一篇文占中谈到的胰岛素抵抗综合征的一部分。为了说明这一点,回到上图中的例子。红线小而密 LDL 较多的人确实患有脂肪肝,空腹甘油三酯为 247 mg/dL。蓝线的人没有脂肪肝,空腹甘油三酯为 87 mg/dL。这些差异并非巧合,因为较高的甘油三酯会增加小而密的 LDL 颗粒的形成。
那么这为什么重要呢?考虑一下,当评估某人心脏病发作或中风的总体风险时,会考虑 ASCVD 的所有主要独立风险因素:高血压、糖尿病、低 HDL 胆固醇,有时还有甘油三酯。一旦考虑了所有这些风险因素,知道 LDL 是小而密还是大而松散并不能提高预测 ASCVD 的能力,不足以证明评估 LDL 大小分布需要花费大量额外成本。这是因为许多这些额外的风险因素与拥有更多小而密的 LDL 密切相关。在某种程度上,已经在风险预测模型中考虑了胰岛素抵抗综合征的重要组成部分,因此添加该综合征的另一个元素,即小而密的 LDL,几乎没有提供任何额外的信息。
小结,是否具有小而密的 LDL 颗粒很重要,但这并不意味着大而松散的 LDL 颗粒无关紧要,如果考虑所有关键风险因素来评估 ASCVD 风险,了解 LDL 颗粒的大小和密度对预测 ASCVD 事件风险的能力几乎没有帮助。
如果仍想了解 LDL 颗粒是否较小且致密,可以使用我在上一篇文章中讨论的胰岛素抵抗综合征海报。如果胰岛素抵抗和甘油三酯位于橙色或红色部分,可以假设您有一些或很多小而致密的 LDL 颗粒。也可以直接测量:只需谷歌搜索 NMR LipoProfile 即可找到美国市场上可买到的检测。正如这里所述,我认为这不是必要的,因为对整体 ASCVD 风险评估贡献不大。
**说法 4:其他风险因素比 LDL 胆固醇更重要**
再来谈谈另一个说法,那就是其他风险因素,如胰岛素抵抗或代谢健康,比 LDL 胆固醇更重要。因此,该说法是,如果代谢健康,可以安全地忽略 LDL 胆固醇。
我不同意可以安全地忽略 LDL 胆固醇,但我同意,综合起来,围绕胰岛素抵抗的风险因素可能更为重要。因为,正如上一篇文章中详细讨论的那样,胰岛素抵抗综合征与空腹甘油三酯升高和 HDL 胆固醇降低、高血压、低度慢性炎症和 2 型糖尿病密切相关。此外,胰岛素抵抗综合征也常常会轻微升高 LDL 胆固醇,导致向更小、更密集的 LDL 颗粒转变。所以,我同意胰岛素抵抗综合征可能是 ASCVD 几个主要风险因素中最严重的集合。用一个例子来说明这一点:
还记得上一篇文章中提到的乔普通先生吗?乔先生今年 65 岁,肥胖,患有 2 型糖尿病、高血压、甘油三酯和 LDL 胆固醇升高以及 HDL 胆固醇降低。这些常见风险因素都以某种方式与胰岛素抵抗或其主要原因有关,其中包括低度慢性炎症和内脏脂肪和异位脂肪过多。他未来 10 年心脏病发作的风险为 39.4%。
假设他担心心脏病风险和糖尿病,开始严格的生酮饮食。在接下来的一年里,他减掉了大部分多余体重,糖尿病也得到了缓解。他的血压也下降了,空腹甘油三酯和HDL恢复正常,但LDL增加更多。对于长期坚持生酮饮食的人来说,这种情况并不少见。然而,任何饮食的结果都有很大差异,所以有些人对生酮饮食的反应可能不太好,而且并不是每个人都会出现LDL水平大幅上升的情况。然而,乔先生的这些变化并不罕见。
乔普通先生在采用生酮饮食大幅减肥之前和之后的对比照。
那么他患心脏病的风险又会如何呢:尽管 LDL 胆固醇水平上升,但心脏病发作风险却大幅下降,10 年后降至 14.5%。所以是的,这部分是正确的:需要综合考虑所有风险因素,即使 LDL 胆固醇水平上升,也完全有可能大幅降低风险。然而,这并不意味着应该忽视 LDL 胆固醇。即使代谢状况得到改善、糖尿病得到逆转、血压降低、HDL 胆固醇水平提高,LDL 胆固醇水平达到 240 mg/dL 也并不理想。假设他的 LDL 胆固醇水平在 70 mg/dL 左右,那么 10 年后他的风险将降至 8.7%。
另一个相关的说法是,LDL 胆固醇只是胰岛素抵抗人群中重要的 ASCVD 风险因素。在这种情况下,值得考虑进行专门研究,以评估 LDL 胆固醇与动脉粥样硬化之间的关系,特别是在总体风险因素非常低的代谢健康个体中。例如,在西班牙进行的PESA 研究表明,即使在没有任何代谢功能障碍证据的年轻无症状个体中,LDL 胆固醇与亚临床动脉粥样硬化之间也存在线性关系。同样,库珀中心纵向研究也发现,在 ASCVD 风险总体非常低的男性和女性群体中,LDL 胆固醇水平与 10 年 ASCVD 风险密切相关。
同时,应该注意的是,即使是这些低风险人群的研究也没有表征重要的代谢因素,例如胰岛素敏感性,通常只是关注糖尿病或高血压等临床因素。因此,LDL 胆固醇和 ASCVD 之间的关系是否会因完美的胰岛素敏感性而改变仍有些不清楚。然而,在缺乏完美数据的情况下,使用目前可用的次优数据作为最佳估计似乎是明智的,这将使我们得出结论,胰岛素敏感参与者的整体 ASCVD 风险会较低,因为通常不会接触一些常见的风险因素(糖尿病、高血压、甘油三酯升高、低 HDL 胆固醇、低度慢性炎症),但 LDL 胆固醇和 ASCVD 风险之间的关系不会在该人群中发生根本改变。
我希望这是有道理的:LDL 胆固醇或载脂蛋白 B 不应被视为万能药,但代谢健康也不应被视为万能药。如果我们重视健康,就应该同时考虑所有风险因素,而 LDL 胆固醇或更确切地说,载脂蛋白 B 显然是关键风险因素之一。
**说法 5:低碳水饮食或生酮饮食导致的 LDL 胆固醇升高不会导致动脉粥样硬化**
很多人都在进行低碳水饮食或生酮饮食,所以我想花点时间来解决这个问题。本质上,这种说法是,像之前的例子一样,像普通人乔先生这样进行生酮饮食的人,可以忽略他升高的 240 毫克/分升的LDL水平,因为他不会因此遭受任何负面影响。
首先我要明确说明,我不知道有任何证据,甚至没有任何潜在机制或假设表明,对于像乔先生这样的人来说,低碳水饮食会使 LDL和 ASCVD 之间的关系有所不同。正如我上面所解释的那样,由于体重正常化、糖尿病和高血压逆转、甘油三酯降低和 HDL升高,66 岁乔先生比65岁的乔先生 患 ASCVD 的风险将大大降低 。没有人应该否认这一点。但是,升高的 LDL仍应被视为风险因素,理想情况下应降低 LDL以进一步降低 ASCVD 风险。对黑客,用科学的话说:我没有看到任何证据或合理的机制表明低碳水饮食可以成为 LDL 和 ASCVD 风险之间关系的效应调节剂。
话虽如此,但有些采用生酮饮食的人表现出一种特殊的表型,值得进一步讨论。这种表型由 戴夫 Dave Feldman、尼克 Nick Norwitz 团队描述过,称为瘦体超敏者(LMHR) 表型。LMHR 是指身材瘦削的人,在混合饮食中 LDL 胆固醇水平正常,但在生酮饮食中 LDL 胆固醇浓度会超过 200 mg/dL,有趣的是, HDL 胆固醇浓度也非常高,为 80 mg/dL 以上,甘油三酯水平低,为 70 mg/dL 以下。
考虑到这些标准,乔先生不符合 LMHR 标准,因为甘油三酯太高,而 HDL 胆固醇太低。但是,如果 乔先生在生酮饮食中减重一点,使 BMI 达到 22,甘油三酯会下降到 50 mg/dL,而 HDL 胆固醇会上升到 90 mg/dL,他就会成为典型的瘦体超敏者。只需将这些略微改变的数字输入心脏病风险计算器,就可以立即看到这些变化会进一步降低他的心脏病风险,在 10 年内降低 12%。所以,具有 LMHR 表型的人的更有利的血脂状况会对整体 ASCVD 风险产生有益的影响。
然而,戴夫和尼克提出了一个假设,即瘦体超敏者中 LDL 胆固醇浓度大幅升高所导致的 ASCVD 风险可能比传统风险评估模型所显示的还要低。换句话说,他们认为,对于具有这种特定表型的人来说,升高的 LDL 胆固醇水平可能不太容易导致动脉粥样硬化。
他们为什么会这么想?毕竟,这是我能想到的第一个如此大幅升高的 LDL 胆固醇水平不会与 ASCVD 风险同样增加的情况。戴夫和尼克已经指出,我认为是正确的,这些 LMHR 中的脂质和脂蛋白代谢非常独特,并且没有关于 LDL 胆固醇与 ASCVD 风险之间关系的数据,这些数据是在与这种表型有一点点相似的人群中产生的。这是因为他们的 LDL 胆固醇升高不是因为脂蛋白处理存在基因缺陷,就像 LDL 基因升高的人一样,而是因为脂蛋白在体内运送更多的脂肪,因为脂肪是生酮饮食的主要燃料来源。所以他们认为这主要是对生酮饮食后身体燃料使用变化的一种代谢适应。这种适应的明显迹象是高 LDL 胆固醇水平与异常高的 HDL 胆固醇水平和低甘油三酯的这种非常不寻常的组合。我个人认为这是一个公平的评估,因为除了采用生酮饮食的精瘦、代谢健康的人之外,确实从未见过这种组合,而且通常不会在胆固醇水平遗传升高的人身上看到。当然,LDL 胆固醇升高的原因是否与相关的 ASCVD 风险有关是一个完全不同的问题。
我还要补充一点,要成为瘦体超敏者 LMHR,饮食和生活习惯可能必须与一般人群截然不同:我还没有看到太多这方面的数据,但我猜想 LMHR 会大量锻炼,很少吃垃圾食品或含糖或酒精的饮料。否则,就无法通过生酮饮食成为瘦体超敏者,因为实际上并不瘦,也不采用生酮饮食。所以,出于这些原因,我确实同意戴夫和尼克已经确定了具有非常独特表型的人。我认为他们的假设很有趣,即生酮饮食中 LMHR 的 LDL 胆固醇水平升高可能不会导致动脉粥样硬化发展,或者至少不会像想象的那样严重,这当然值得研究。
值得赞扬的是,戴夫和尼克发起了一项小型众筹试点研究,研究对象是 100 名瘦体超敏者,平均已经进行生酮饮食 4.7 年。研究的总体目标是评估他们是否会随着时间的推移而形成动脉粥样硬化斑块。这将通过重复 CT 血管造影来评估,以量化冠状动脉钙沉积和冠状动脉斑块的数量。该研究的主要纵向结果仍未公布(见下图)。
设计一项纵向(待定)和横断面研究,探讨生酮饮食中瘦体超敏者(LMHR)中 LDL 胆固醇大幅升高对动脉粥样硬化的影响。
但是,该团队已完成基线数据收集,包括冠状动脉钙化和冠状动脉斑块的测量。然后,他们将这些 LMHR 中的 80 个与另一项现有队列研究(迈阿密心脏研究)的参与者进行匹配。这里的目标是根据主要 ASCVD 风险因素(血清脂质谱除外)匹配参与者。正如在下表中看到的,这些组在年龄、性别、种族以及所有主要 ASCVD 风险因素(BMI、总胆固醇、LDL 胆固醇和 HDL 胆固醇以及甘油三酯除外)方面都匹配良好。但是,所有这些都是 LMHR 表型的一部分,因此这种差异是设计使然。就主要 ASCVD 风险因素而言,根据设计,主要差异在于 LDL 胆固醇和 HDL 胆固醇水平,生酮饮食的 LMHR 平均 LDL 胆固醇为 272 mg/dL,而匹配的对照组为 123 mg/dL。这当然是一个相当大的差异,根据我们所知,由于LDL大幅升高,生酮饮食者的动脉粥样硬化进展应该更快。事实上,由于这些饮食者已经平均暴露于高密度脂蛋白胆固醇水平 4.7 年,他们可能已经比对照组有更多的冠状动脉斑块。
对接受生酮饮食的 LMHR 表型的参与者与 80 名 LDL 胆固醇水平低得多但其他主要 ASCVD 风险因素相匹配的非 LMHR 参与者进行了比较。
评估是否确实如此是在基线进行横断面分析的目的。首席研究员 Matthew Budoff 博士在上周(2023 年 12 月 8 日)的一次会议上介绍了结果。值得注意的是,经过 4.7 年的生酮饮食后,CT 血管造影数据显示这两组在冠状动脉钙化评分或冠状动脉斑块评分方面没有任何差异。尽管平均 4.7 年内 LDL 胆固醇水平显著升高,但超过 50% 的生酮组的总斑块评分仍为零。现在,这是一个有趣的发现,似乎支持戴夫和尼克的假设,即生酮饮食的 LMHR 中这些单独的 LDL 升高不太会致动脉粥样硬化。但是,我确实认为需要进行细致的讨论才能从这些结果中得出正确的结论。 (顺便说一句,如果想听这些研究人员讨论他们的横断面研究结果,这里有他们最近接受的采访的链接)。
首先,我在网上看到很多脂质学家或心脏病学家的评论,他们说 4.7 年的平均 LDL 胆固醇水平(分别为 272 和 123 mg/dL)不可能导致冠状动脉钙化或斑块的差异。他们中的许多人认为这些数据完全没有意义。
那么解答一下这个断言。我会说,是的,当然,如果这是生命中的前 4.7 年,那么这太短了。动脉粥样硬化斑块可以在不到 5 年的时间内形成,但这需要更高的 LDL 胆固醇水平。然而,这并不是这些参与者生命中的前 4.7 年。相反,在 LMHR 组和匹配的对照组中,在这次基线评估之前的 4.7 年,两组的平均年龄约为 50 岁,我们可以假设他们在此之前对 LDL 胆固醇的暴露程度相似。可能如下图所示,平均而言。请记住,重要的是一生中对 LDL 胆固醇的累积暴露,到他们 50 岁时,两组的参与者已经积累了大量的 LDL 胆固醇暴露。可能大约是 5,000 mg/dL 年,这被认为是 ASCVD 风险开始显现的阈值。
我是怎么得出每年 5,000 mg/dL 的?这看起来好像他们生命前 50 年的平均 LDL 胆固醇浓度约为 100 mg/dL , 乘以 50年,得出 50 岁时每组参与者的平均累积终生暴露量:每年 5,000 mg/dL。希望这说得通?
与迈阿密心脏研究 (红线) 中的对照组相比,采用生酮饮食 4.7 年显著提高了具有 LMHR 表型的人 (绿线) 的 LDL 胆固醇的终生累积暴露量。 (图表显示的是估计暴露量,并非基于实际数据)。
因此,当 LMHR 开始生酮饮食时,这已经是估计的 LDL 终生暴露量。然后他们开始生酮饮食,他们的 LDL 飙升至约 270 mg/dL。至少,这是最佳估计。所以现在,在 55 岁,也就是进行这项基线评估的时候,在 LDL 总体累积终生暴露量方面确实存在相当大的差异(上图中用黄色阴影表示)。所以我不同意不可能看到差异。在我看来,总的终生累积 LDL 胆固醇暴露量肯定已经将一些 LMHR 提升到我们看到动脉粥样硬化大量快速发展的区域,而且比匹配的对照组更有可能出现这种情况。
同时,我确实认为必须承认生酮饮食的时间可能太短。还需要明确的是,这是一项小型试点研究的横断面基线分析。这些数据很有趣,很有希望,但只是漫长过程的第一步,希望这段过程包括对这些参与者进行至少 5 年、最好 10 年的长期随访,理想情况下,还有第二次更大规模的研究,然后才能有充分的理由和信心地得出结论,LMHR 中升高的 LDL 胆固醇浓度确实不太容易致动脉粥样硬化。时间在这里是一个重要因素,我最好的估计仍然是 LMHR 形成动脉粥样硬化斑块的速度将高于匹配的对照组。如果我错了,我会很高兴,但这是我目前最好的估计。
因此,还需要明确,这些数据丝毫不影响对 LDL 胆固醇在 ASCVD 风险中的作用的总体理解,正如我在网上看到一些人所建议的那样。现在拥有大量来自动物、观察和遗传研究的证据,甚至来自超过 200 万参与者的随机对照高质量试验的数据,而一项 160 名参与者的试点研究的横断面基线数据肯定无法改变我们对 LDL 胆固醇与 ASCVD 之间关系的总体理解。因此,断言这些数据对脂质心脏假说提出了质疑是愚蠢至极的。
这项调查的价值在于,脂质和脂蛋白表型在 LMHR 中确实非常不寻常,而且 LMHR 几乎肯定也拥有异常健康的生活方式。这提供了从根本上了解脂质代谢及其与 ASCVD 的关系或 ASCVD 总体情况的可能性。例如,如果我们发现这些大幅升高的 LDL 胆固醇浓度即使在较长时间内也不会导致 ASCVD 的预期进展,或者进展速度比预期慢得多,情况就会如此。也许生酮饮食的 LMHR 中 LDL 颗粒的组成或代谢有些特别,或者导致某些具有 LMHR 表型的其他饮食或生活方式因素在某种程度上非常具有保护作用。我确实认为我们应该对这些可能性持开放和好奇的态度。
因此,总的来说,我对这项研究感到很兴奋,希望研究人员能够纵向跟踪这些 LMHR,理想情况下至少再跟踪 5 年,最好是 10 年。理想情况下,开始另一个样本量更大的队列。与此同时,我重申,我认为谨慎的做法是假设 LDL 胆固醇和 ASCVD 风险之间的关系在这个人群中成立,直到拥有更可靠的数据。尽管这些呈现的基线数据很有希望,但太有限了,不能被视为确凿的证据。换句话说,这些基线数据并没有改变我对 LDL 胆固醇在 ASCVD 中的作用的看法,无论是一般意义上还是在生酮饮食的 LMHR 中。尽管我对这个假设很感兴趣,但我当然不会拿我的生命打赌这在现在是正确的。如果我在生酮饮食过程中出现 LDL 胆固醇大幅升高的情况,我会调整饮食以降低 LDL 胆固醇水平,或寻求降脂疗法。
最后,让我再次声明,关于 LMHR 的假设不应推广到其他生酮或低碳水饮食的人。如果遵循低碳水或生酮饮食,并且 LDL 胆固醇升高,但不是很瘦,或者 HDL 也低,或甘油三酯高,或其他风险因素,如吸烟或肾脏疾病,我认为在这里讨论的都不适用。除了这种非常具体的 LMHR 表型之外,我不知道低碳水或生酮饮食可以通过什么机制改变 LDL 胆固醇对 ASCVD 风险的影响。即使对于 LMHR,请记住,目前正在研究一种处于临床测试早期阶段的假设。
**说法 6:胆固醇不会有害,因为是人体产生的天然物质,并且是许多重要功能所必需的**
现在来解决最后一个说法,那就是胆固醇不会有害,因为是人体产生的天然物质,并且是许多重要功能所必需的。
如果看过我的其他文章,也许能够回答这个问题。难道就没有天然的、人体可以制造的、在人体中发挥重要作用的物质,如果在我们血液中的浓度过高,仍然会增加患慢性病的风险吗?
是的,当然有无数种这样的物质。葡萄糖就是一个很好的例子,与胆固醇相似:葡萄糖当然是一种天然物质。如果葡萄糖下降太多,人就会死亡,因此,葡萄糖对人的生存至关重要,因此,可以放心地认为具有重要的功能。如果摄入的葡萄糖不足,身体就会内源性地产生。但如果血液中葡萄糖过多,比如糖尿病,患慢性病的风险就会增加。或者是胰岛素,是天然的,身体可以制造,但太少或太多都会让人死亡。需要血液中适量的葡萄糖和胰岛素来保持长期健康。太少或太多都会有问题。为什么对葡萄糖、胰岛素和无数其他物质都接受这一点,但对于胆固醇,却一直认为对细胞膜很重要,是激素或胆汁酸合成的重要底物,所以血液中胆固醇过多不会有害?这很令人困惑,希望你能看出这是一个愚蠢的论点。
不过,还是要讨论一下低 LDL水平是否与负面健康后果有关。现有数据确实表明,虽然某些降脂药物可能会产生不良影响,但这些影响本身与 LDL 胆固醇水平过低无关,事实上,在极端降脂情况下将 LDL 降低至 11-45 mg/dL 并未发现与负面健康后果有关。这与由于遗传原因 LDL 胆固醇水平同样非常低的个体的情况一致,似乎也没有遭受任何负面健康后果。
**总结和结论**
总之:现有证据清楚、一致且强烈地支持了载脂蛋白 B 在 ASCVD 发展中起因果作用的观点。明确地说,证据是压倒性的,我发现一些网红名人只是用通常相当肤浅或考虑不周的论点将极其有力和一致的数据抛在一边,这是非常令人担忧、不幸的,而且可能非常有害。
因此,我强烈建议定期测量空腹血浆载脂蛋白 B 浓度,使用载脂蛋白 B 指导营养或药物治疗。非HDL(通过从总胆固醇中减去HDL来评估)或LDL是很好的替代测量方法。对于载脂蛋白 B 和LDL,在初级预防中,低于 80 mg/dL 的水平是最佳的。对于非HDL,我的目标是 100 mg/dL 以下的浓度。免责声明:这些不是官方指南,而是我对 ASCVD 一级预防这些浓度的看法的综合。请注意,二级预防(即心脏病发作或中风的患者)的目标通常较低。
我还建议一生中至少测量一次 Lp(a),以改善 ASCVD 风险预测并指导治疗。如果 Lp(a) 升高至 30 mg/dL 以上,尤其是 50 mg/dL 以上,则应更严格地控制其他 ASCVD 风险因素。
在其他与脂质相关的风险因素中,定期评估 HDL和甘油三酯也是有益的,这些既是 ASCVD 风险因素,也是监测胰岛素抵抗综合征出现的便捷措施,如上一篇文章所述,我已将其链接在下面。对于 HDL,男性的最佳浓度为 60 mg/dL 以上,女性的最佳浓度为 70 mg/dL 以上。
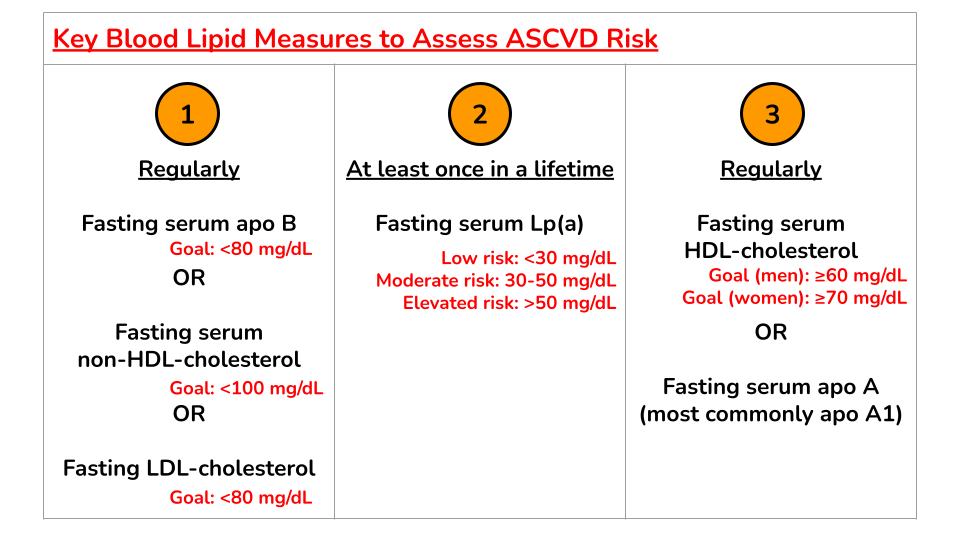 血脂目标浓度以最大限度地降低 ASCVD 的风险(一级预防)。
血脂目标浓度以最大限度地降低 ASCVD 的风险(一级预防)。
在讨论完脂质相关风险因素后,我想再次强调,ASCVD 是一种多因素疾病,在风险评估和指导治疗时使用所有已知的独立风险因素至关重要。这些因素包括年龄、性别、种族、糖尿病、高血压、吸烟、慢性炎症、慢性肾病、高密度脂蛋白胆固醇、脂蛋白 (a) 和载脂蛋白 B 或非HDL或LDL。
在评估 ASCVD 风险时,请特别认真考虑,对于每个风险因素而言,最重要的是暴露量乘以暴露时间。这一系列研究强烈表明,早期干预和(甚至更好的)预防是最大限度减少所有这些风险因素的终生暴露的关键。
最后,我要强调的是,本文不是药物的宣传。事实上,本网站的主要目标之一是帮助人们在不需要药物的情况下过上长寿健康的生活。我写本文的目的只是提供关于如何使用血脂来评估 ASCVD 风险的公正指导。药物是否有助于降低升高的风险当然需要由经验丰富的医生根据患者逐一进行评估,最好是在考虑了其他降低风险的方法并仔细讨论了药物的副作用之后。因此,很明显,药物可能是一种有用的选择,但在我看来,最好是在生命早期养成良好的饮食、运动和生活习惯,以尽可能长时间地将可以影响的所有风险因素保持在最佳或接近最佳的范围内。这将最大限度地降低 ASCVD 的风险,而无需任何药物。如果这些风险因素中的任何一个已经升高,我认为我们仍然应该优先解决根本原因,这通常包括不良饮食、长期暴饮暴食、久坐的生活方式、睡眠不足和长期压力。除此之外是否需要药物治疗需要由你和你的医生决定。
这是一篇很长的文章,感谢您的耐心阅读。我非常希望本文能解答您的所有问题,消除您可能存在的任何困惑。如果您还有任何问题,请随时留言。我也希望本文不是太技术性。请随时给我一些反馈。
**参考**
- 费恩戈尔德。脂质和脂蛋白简介。Endotext 2021。
- 金斯伯格。脂蛋白生理学。北美内分泌代谢诊所 1998;27:503-19。
- Ference 等人;低密度脂蛋白导致动脉粥样硬化性心血管疾病。1. 来自遗传、流行病学和临床研究的证据。欧洲动脉粥样硬化学会共识小组的共识声明。欧洲心脏杂志 2017;38:2459-72。
- Wiegman 等人;儿童和青少年家族性高胆固醇血症:通过优化检测和治疗延长寿命。欧洲心脏杂志 2015;36:2425-37。
- Horton 等人;PCSK9:一种协调 LDL 分解代谢的转化酶。《脂质研究杂志》2009;50 增刊:S172-7。
- Masson 等人;非他汀类降脂治疗在冠状动脉粥样硬化消退中的作用:荟萃分析和荟萃回归。《健康与疾病中的脂质》2020;19: 111。
- Ference 等人;PCSK9 和 HMGCR 的变化与心血管疾病和糖尿病风险。新英格兰医学杂志 2016;375:2144-53。
- 利比。动脉粥样硬化的变化情况。《自然》2021;592:524-33。
- Sniderman 等人;载脂蛋白 B 颗粒与心血管疾病:叙述性综述。JAMA Cardiology 2019;4:1287-95。
- Cole 等人;精准医疗时代载脂蛋白 B 的应用:是时候改变范式了吗?临床医学杂志 2023;12:5737。
- Bilgic 和 Sniderman。低密度脂蛋白胆固醇、非高密度脂蛋白胆固醇和载脂蛋白 B 用于心血管护理。Current Opinion in Cardiology 2024; 39: 49-53。
- Kronenberg 等人;动脉粥样硬化性心血管疾病和主动脉瓣狭窄中的脂蛋白 (a):欧洲动脉粥样硬化学会共识声明。《欧洲心脏杂志》2022;43:3925-46。
- Schoch 等人;动脉粥样硬化性心血管疾病中高密度脂蛋白胆固醇的最新进展。动脉硬化临床研究 2023;35:297-314。
- Farnier 等人;甘油三酯与动脉粥样硬化性心血管疾病风险:最新进展。心血管疾病档案 2021;114:132-9。
- Krauss。小而密的低密度脂蛋白颗粒:临床相关性?《脂质学当前观点》2022;33:160-6。
- Rizvi 等人;脂蛋白和心血管疾病:致动脉粥样硬化小而密的 LDL 的临床意义和新的治疗选择的最新进展。生物医学 2021;9:1579。
- Tsai 等;小而密低密度脂蛋白胆固醇的新自动化检测可识别冠心病风险。动脉粥样硬化的多民族研究。动脉硬化血栓形成和血管生物学 2014;34:196-201。
- Ibanez 等人;早期亚临床动脉粥样硬化 (PESA) 研究进展。《美国心脏病学会杂志》2021;78:156-79。
- Abdullah 等人;低密度脂蛋白胆固醇与 10 年动脉粥样硬化性心血管疾病风险较低的人群心血管死亡率的长期关联。《循环》2018;138:2315-25。
- Norwitz 等人;限制碳水化合物饮食导致 LDL 胆固醇升高:“瘦体超敏者”表型的证据。《营养学最新进展》2021;6:nzab144。
- Norwitz 等人;脂质能量模型:在限制碳水化合物饮食的背景下重新想象脂蛋白的功能。代谢物 2022;12:460。
- Ference 等人;脂质对心血管健康的影响。《美国心脏病学会杂志》2018;72:1141-56。
- Sabatine 等人;对于从极低水平开始的患者,进一步降低低密度脂蛋白胆固醇的有效性和安全性:一项荟萃分析。JAMA Cardiology 2018;3:823-8。
https://nourishedbyscience.com/blood-lipids-and-cvd-risk/
Edit:2024.10.12
- 泰勒 说:
- *2023 年 12 月 17 日凌晨 2:46 这可能是我过去 10 年里读过的关于这个主题的最好的科学交流和解释。干得好,谢谢你整理这些!请继续发表这样的文章。 - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2023 年 12 月 17 日上午 11:55 谢谢你,泰勒。 - 7cb2e0235f5f70240113509328cdbcb7凯伦·拉文 说: 2023 年 12 月 17 日上午 7:57 这是一篇写得很好、详细且易于理解的文章,解释了目前公认的关于脂质和 ASCVD 的科学。这显然需要花时间整理和撰写。插图也非常有用。感谢您的所有努力。这应该是所有播客的必读内容,但他们告诉听众 LDL 升高不会对重大心血管事件造成长期风险。 - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2023 年 12 月 17 日上午 11:55 谢谢,Karen。我认为问题在于,无论向他们展示什么证据,大多数播客都不会改变主意。问题在于,提出这些论点太容易了:例如,降脂试验中短期绝对风险降低率低的问题是正确的,而且很容易验证。因此,很容易做出看似正确的陈述,然后稍微扭曲结论,让“我们被骗了”或“这一切都是为了大制药公司和大笔金钱”看起来是理所当然的…… 祝好, Mario - b720164f72a40eeae83fbc868cfb523f莉丝 说: 2023 年 12 月 17 日下午 7:10 太棒了!我读了每一个字。 - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2023 年 12 月 17 日下午 10:34 谢谢你! - fadc1d22e5429fda769485bcf32f6c65Bernhard Boser 说: 2023 年 12 月 17 日下午 9:16 感谢您对这个主题的精彩演讲。我有两个问题希望您能解答一下: - 您引用了 FH 作为 LDL-C 与 ASCVD 因果关系的主要证据。如果我理解正确的话,FH 会阻止 LDL 从血液中正常循环。对于大多数人来说,这不是 LDL 升高的原因。在这种情况下,类比仍然成立吗? - 您建议尝试生活方式干预来减轻 ASCVD 风险。虽然饮食措施和运动对改善代谢健康、降低血压等非常有效,但不幸的是,这些通常不会降低 LDL,在某些情况下甚至会增加 LDL。有哪些非药物措施可以降低 LDL-C 引起的风险? 谢谢!Bernhard - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2023 年 12 月 17 日下午 10:46 你好,Bernhard, 很好的问题。 1.) 您提出的担忧是合理的,而且一些 FH 患者可能确实存在其他脂质和脂蛋白处理障碍,这可能会导致 ASCVD 风险增加。然而,有趣的是,有几种不同的基因突变会导致 LDL 胆固醇升高和 ASCVD 风险增加,并且 ASCVD 风险的增加与 LDL 胆固醇水平相当一致。如果这些基因突变的影响大多与 LDL 胆固醇无关,而是其他一些不太明显的分子机制,那么人们会认为 LDL 胆固醇和 ASCVD 风险之间的关系会更加随机和混乱。尽管如此,我们仍然无法 100% 确定任何证据证明罪魁祸首确实是 LDL 胆固醇,或者更确切地说是载脂蛋白 B 的脂蛋白。因为即使在临床降脂试验中,人们也可以证明他汀类药物对身体的其他作用不仅仅是降低脂质,这可以部分解释其对 ASCVD 风险的影响。然而,考虑到大量不同的证据,而且这些证据在人群和不同研究领域中非常一致,该领域的共识是,含载脂蛋白 B 的脂蛋白可能是因果关系。例如,可以在他汀类药物和 PCSK9 抑制剂靶基因中找到遗传变异,这些遗传变异恰好模仿了他汀类药物和 PCSK9 药物对 LDL 胆固醇和 ASCVD 风险的影响(文章中参考文献 7)。其中一些证据的一致性非常惊人。 关于 2.) 将在未来的视频中详细讨论这一点,但总的来说,纤维含量和脂肪酸组成在调节载脂蛋白 B 和 LDL 胆固醇方面起着重要作用。减少反式脂肪酸和长链饱和脂肪酸,增加不饱和脂肪酸是一种可以产生相当大影响的饮食变化。增加纤维是另一种。对于生酮饮食的人来说,每餐多吃一点碳水化合物可以产生巨大的影响。最后,避免暴饮暴食和脂肪肝是保持血脂(包括甘油三酸酯和 LDL 胆固醇)较低的关键方面。我在这些文章中谈到了这一点: <https://nourishedbyscience.com/personal-fat-threshold/> <https://nourishedbyscience.com/insulin-resistance-syndrome/> 祝好, 马里奥 - fadc1d22e5429fda769485bcf32f6c65Bernhard Boser 说: 2023 年 12 月 18 日下午 9:49 嗨,Mario,非常感谢您的深刻。我期待未来视频中讨论除降脂药物之外的降低 ASCVD 风险的替代方案。 关于 1) – 我可能弄错了,但据我所知,与 FH 相关的一种遗传缺陷是减少或抑制清除血液中的 LDL。这与高 LDL 的更常见原因(例如暴饮暴食或脂肪肝以及可能的胰岛素抵抗)不同。 我看到过一些论点,认为长时间处于循环中的 LDL 可能会“受损”,受损的 LDL 会导致 ASCVD,而有效清除的 LDL 则风险较低(您的视频中也提到了这一点,比较了“A”型和“B”型脂质模式)。LMHR 研究的初步结果为这一假设提供了一些可信度:这个群体似乎受到高水平 LDL 的影响,但动脉粥样硬化似乎较少。 如果 LMHR 研究(目前只有一项,第二项正在规划阶段)取得成功,可能会开辟一条降低 ASCVD 风险的新途径,而不需要药物或饮食干预,例如用不饱和脂肪代替饱和脂肪(这本身就有很多问题,尤其是植物油)。不过,我同意,生酮饮食需要付出很多努力,并不适合所有人。如果有效的话,服用药丸肯定是一条更简单的途径。 我希望您不要将此解读为批评——但我仍然对 ASCVD 风险因素和缓解策略感到困惑,并且觉得我们对这个问题的了解比大多数从业者承认的要少。 - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2023 年 12 月 19 日下午 5:56 关于你的最后一句话:我重视良好、尊重的辩论,如果有人得出不同的结论,我完全没问题。 我也理解您的印象,即我们对这个问题的了解程度比大多数从业者承认的要少。然而,从我的角度来看,我们确实非常非常了解这个过程,而且在这个领域工作的科学家和临床医生中,对于社交媒体上某些群体不断提出的大多数观点,并没有太多的争论。是的,当然,有些问题我们需要更多的数据。但是,我会诚实地告诉你:我在社交媒体上听到的大多数说法都没有经过深思熟虑,正如我试图在这篇博文中展示的那样。社交媒体上关于这个话题的很多内容让我想起有人说“好吧,它看起来像一只鸭子,嘎嘎叫得像鸭子,摇摇摆摆地走着,游泳也像鸭子,但在这种情况下,它可能仍然是一只小天鹅”。 从我的角度来看,有两个值得探讨的问题我们还没有确切的答案,而社区对更多数据的兴趣也是正确的: (1.) 在没有任何触发事件(内皮功能障碍、炎症、高血压、氧化应激)导致内皮损伤,且没有任何其他风险因素的情况下,升高的 LDL 胆固醇是否会导致动脉粥样硬化斑块。在我看来,这些问题尚未得到充分研究,因此无法确定。同时,很明显,无一例外,每个人都会在其生活中接触到其他一些风险因素,无论是空气污染还是因感染引起的暂时性急性炎症,所以我认为这个问题在学术上很有趣,但并不否认我们从较低的 apo B 中受益。即使是 LMHR,例如,假设 LMHR 是无害的,也可能出现与高血压和炎症相关的健康危机:那么极高的 LDL 胆固醇水平会对他们的内皮造成什么影响?一旦斑块形成,如果 LDL 胆固醇保持较高水平,它就会增长。 (2.) 特殊的 LMHR 表型是否与动脉粥样硬化无关,或者与动脉粥样硬化的发生率低于我们的预期。我仍然持怀疑态度,但我认为这是一个值得研究的问题。 祝好 马里奥 - 04e4b143d4fa50da59a3dced533240bf安德烈 说: 2023 年 12 月 17 日下午 10:05 马里奥,从视觉冲击力来看,整体演示非常出色。我赞赏你的努力。但是,对我来说,对说法 #2 的揭穿根本无法令人信服;基于假设,而不是证据;你假设如果我们跟踪这些患者几十年而不是几年,相对风险就足够好了;你似乎忘记了 JUPITER 试验持续了不到 2 年;你同意吗——只要不到 2 年就足够好了,让我们继续下去,希望一切都好? - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2023 年 12 月 17 日下午 10:29 一旦先验定义的临床益处在统计学上得到证实,我们就有道德义务停止随机对照试验。这就是研究的样本量和持续时间所基于的。世界上没有一个道德委员会会允许大约一半的参与者(通常是 ASCVD 高风险患者)在降低临床风险的有效性得到证实后继续服用安慰剂。因此,我们永远不会知道 10 年或 20 年后风险降低的实际程度。然而,我最好的猜测是,相对益处实际上会随着时间的推移而增加,因为存在累积终生暴露的问题,而这种差距也会随着时间的推移而扩大。 我个人认为这是该领域中代表性最差、误解最多的主题之一。正如我在视频中所说,考虑到一生中累积的载脂蛋白 B 粒子暴露量才是最重要的,而不是当前的浓度,我们甚至可以如此迅速地检测到降脂治疗的效果,这一事实充分说明了这些粒子在 ASCVD 中发挥的关键作用。 最好的, 马里奥 - 04e4b143d4fa50da59a3dced533240bfAndrei Croitoru 说: 2023 年 12 月 18 日下午 5:40 道德义务?又基于什么?假设?希望?这和“相信科学”没什么不同。如果我们援引哲学论点,我有几个可以给你(还有更多,但我只坚持这两个): – 莫尼兹于 1949 年因脑白质切除术获得诺贝尔奖。我们是不是应该说,当时剥夺患者接受脑白质切除术的权利是不道德的,对吧? – 精神疾病的胰岛素冲击疗法;持续了几十年。不做不道德,对吧? 希望和假设违反了卡尔·波普尔的证伪理论,该理论认为,要将一个理论视为科学,必须能够被检验,并可以证明其错误。出于“道德目的”而过早停止试验是非常不道德的,因为破坏了被证明错误的可能性。 真挚地, 安德烈 - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2023 年 12 月 18 日下午 7:21 我认为你误解了:如果你进行试验,你必须先确定(在你招募第一位参与者之前)你的假设是什么,你认为治疗组和安慰剂之间具有临床意义的差异变化是什么,以及你的样本量是多少以及理由是什么。例如,一旦降脂试验表明已经达到 ASCVD 减少的主要终点,即使在短期内绝对益处很小,研究人员在道德上也有义务停止试验。因为继续不向安慰剂组提供有效治疗是不道德的。例如,一旦临床益处得到证实,美国或德国的任何道德委员会都不会允许研究人员继续不向随机接受安慰剂治疗的人提供有效治疗。 过去 50 年来,生物医学研究的标准显然发生了很大变化。50 多年前经常进行的许多研究如今已不再可行。 我只想解释一下为什么我们不进行他汀类药物或 PCSK9 抑制剂与安慰剂的试验,比如说 20 年(听起来你对此持怀疑态度,不是吗?)。以及为什么短期降脂试验中看到的微小绝对益处不容小觑,因为如果通过解决所有关键风险因素将多个这样的短期益处叠加起来,在我看来,长期累积效应将非常有意义。 祝好, 马里奥 - fadc1d22e5429fda769485bcf32f6c65Bernhard Boser 说: 2023 年 12 月 18 日下午 9:26 我想补充一点:他汀类药物的副作用通常需要比试验更长的时间才能显现出来。那么,一种可能的结果难道不是,虽然他汀类药物可以减少 ASCVD,但它可能同时导致另一个问题(例如肌肉或痴呆症)。全因死亡率可能是一个更好的标准,但可能需要在更长的时间内进行评估。 不幸的是,关于他汀类药物副作用的数据很少,解释也存在争议。可以理解的是(尽管可能不符合道德),制药公司并不热衷于资助长期研究来评估可能减少其业务的问题。 由于利益冲突,该领域肯定存在偏见。我的心脏病专家建议我看看 Fourier 试验(依洛尤单抗和心血管疾病患者的临床结果,新英格兰医学杂志,2017 年),作为降脂药物有益的“证据”。LDL-C 的降低确实令人印象深刻(平均 30mg/dL)。我的文献搜索还带来了以下文献:“恢复 FOURIER 心血管疾病患者依洛尤单抗心血管结果试验中的死亡率数据:基于监管数据的重新分析”(BMJ Open,2021 年),该文认为结果没有得到适当报告。作者总结道:“经过重新裁决,在 FOURIER 试验中,依洛尤单抗组的心脏源性死亡率在数值上高于安慰剂组,表明可能存在心脏损害。” 我没有资格评价这些说法,但令我惊讶的是:(1) 这个问题出现在另一份文献中,(2) 原文献的作者几乎没有做出任何反应(除了在回答记者的问题时提出了异议)。在我的科学领域,这类问题的处理方式不同:提出异议,由各方和独立审阅者进行调查,并在同一地点发表结论。 这里的讨论很有价值,因为没有偏见。 - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2023 年 12 月 19 日下午 6:14 是的,我也有同样的担忧,担心长期服药的副作用。这就是为什么我如此重视预防、营养和生活方式。 也感谢您分享傅立叶试验问题。我之前不知道这。稍微阅读一下,现在可能还太早,无法真正知道正确的结果是什么,但这种争议肯定不会让我们中的任何人更渴望服用这些药物……您指出这里涉及的金钱实在太多了,这绝对是正确的…… 干杯 马里奥 - bbae3244ae674ae8f4b5a4a5756e3c0bdlac30314b950f8 说: 2023 年 12 月 19 日下午 6:26 你好, 我刚刚发现您的网站和这篇文章,并希望对这个关于该主题的极其详尽且通俗易懂的介绍表示感谢。我就是您所提到的“普通人”……一个 64 岁的男性,过去几年一直在有意识地改变饮食和生活方式。我的生物标志物中的大部分变化与您在此处列出的非常相似(例如,A1c 从 6.4% 降至 5.3% 等,体重从 215 降至 185 等) 我有一个问题,关于 apo(b) 和 LDLc 之间的对应关系。我的理解是,有时人们会看到两者之间的不一致,LDLc 相对较低,但 apo(b) 升高。这显然说明了检查 apo(b) 的重要性。但就我而言,我的情况似乎更不寻常……apo(b) 相当低,66 mg/dL(低于一年前的 74),LDLc 略有升高,最近的血液检查显示为 123 mg/dL(总胆固醇 198,甘油三酸酯 97)。我目前没有服用他汀类药物或任何其他药物干预,但正在考虑是否有必要这样做。 我是否可以从本质上只关注 apo(b) 数值而忽略 LDLc 数值? 再次感谢, 莫 - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2023 年 12 月 20 日凌晨 1:33 嗨,Mo, 我希望您理解,我无法在此提供医疗建议。我只能重复两位领先的脂质学家在下面链接的论文中所说的话: – Apo B 是比 LDL-胆固醇更准确的 ASCVD 风险指标,因为 Apo B 与重要的指标(含致动脉粥样硬化脂蛋白的 Apo B 数量)成正比,而 LDL-胆固醇仅与致动脉粥样硬化脂蛋白的数量相关 – Apo B 的实验室测量是标准化和直接的,而 LDL-胆固醇最常见的测量是基于总胆固醇、HDL-胆固醇和甘油三酯的计算。因此,Apo B 的实验室测量比 LDL-胆固醇更准确。 <https://pubmed.ncbi.nlm.nih.gov/37934698/> 祝一切顺利, 马里奥 - 4c80be2ede513460ec3f9cb09cd0b02dconeal22002 说: 2023 年 12 月 19 日下午 6:49 嗨,Mario,非常有价值和信息丰富的讲座和笔记。我可能还在吸收,我会在思考后继续回头查看。70 岁了,我现在可以看到事情已经发生了变化。我的 LDL 水平一般较高(121),但 HDL 水平也较高(87),甘油三酯水平较低(56)。这并没有改变,但现在我被认为因为 LDL 水平高而处于更高的风险中,而以前医生对此不以为然,因为我的 HDL 水平高,甘油三酯水平低,我很健康,血压正常或较低。看了你的视频后,我有了更好的理解。非常感谢,Cathy - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2023 年 12 月 20 日凌晨 1:35 嗨,Cathy, 如果医生告诉您,您属于“较高”风险或处于边缘风险,那么最好同时测量 apo B 和 Lp(a)(均取空腹血)以帮助指导治疗决策。 祝好, 马里奥 - a93c40e54cb972bead4978b2e9871babIgor Urbanavichus 说: 2023 年 12 月 20 日上午 6:37 非常感谢这篇文章!既有趣又难读:) 1 – 读完后,我产生了一个想法 – 减少脂肪食物的摄入。问题 → 如果我今年 32 岁,身体瘦弱,没有慢性病,坚持低升糖指数饮食,那么我得出的结论正确吗? 2 – 吃的脂肪们血液中的脂蛋白有多大影响? 3 – 据说植物脂肪比动物脂肪更有害。这是真的吗? 4 – 您在撰写文章时会使用 Chat Gpt 4 吗?它可能是一个非常好的工具,可以让处理文本变得更加容易。可以帮助使测试更简单、更易于阅读。 - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2023 年 12 月 20 日上午 10:25 嗨,Igor, 我将在以后的帖子中回答您的所有问题,如果我在这里给您一个简短的,那我就太肤浅了。抱歉。 不,我没有使用任何人工智能。 干杯, 马里奥 - 4c80be2ede513460ec3f9cb09cd0b02dconeal22002 说: 2023 年 12 月 20 日下午 5:13 感谢您的评论。我只是不确定知道我的 Lp(a) 是否会改变我的轨迹,因为看起来最好的事情仍然是保持健康、合理饮食、减轻压力、睡个好觉。甚至想到测试 Lp(a) 都会让我感到焦虑。我有 3 个姐妹,我们都超过 65 岁,妈妈活到了 98 岁,爸爸活到了 83 岁。家里没有心脏病患者。当我看到我的胆固醇在过去高得多而我的医生却什么也没说时,我感到非常困惑。您的视频确实有助于解释这一点。我也看过这个视频,我认为他们提出了一些非常好的观点。虽然我认为他们在某些观点上有所不同,但在其他方面,他们与您的许多视频一致。改变生活方式是最好的。https: //www.youtube.com/watch? v=yr_4RoPhtu4&t=631s - 4c621fda7bd799be9e16332714e0f7e2保罗 说: 2023 年 12 月 20 日上午 5:45 我很好奇,为什么您怀疑从长远来看,LMHR 会增加 CVD 风险。我的第一个问题是:在看到 LMHR 基线与迈阿密心脏基线的结果之前,您是否预计 LMHR 组的斑块增加为零?根据您的文章,我认为您对最初的发现感到惊讶。那么从逻辑上讲,为什么假设长期结果不会相似是一个很大的想象范围? 其次,正如您正确指出的那样,LMHR 组在饮食坚持和锻炼方面可能是一个相当健康的群体。归根结底,生活就是选择和风险,我认为,将碳水化合物重新纳入饮食或服用他汀类药物等药物对健康寿命的风险可能比 CVD 事件的绝对风险更大。特别是如果您像我一样,碳水化合物会迅速引起渴望,导致过度沉迷于加工食品。 第三,据我所知,HDL 是脂质学中最不为人所知的一块拼图。那么,假设 LMHR 中 HDL 升高正是可能完全消除 LDL 升高风险的机制,这是否有些牵强?是否存在另一种比 LMHR 具有更高 HDL 的表型?如果有,我们可以从中学到什么? - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2023 年 12 月 20 日上午 10:14 嗨,保罗, 这些都是好问题。认为 LMHR 可能是一个例外并不夸张。正如我在帖子中试图解释的那样,LDL-胆固醇和 ASCVD 之间的关联非常强烈且一致,并且根据我们目前对如此大幅升高的 LDL-胆固醇水平的了解,我预计动脉粥样硬化斑块的进展会比 LDL-胆固醇水平较低的代谢健康人群更大。 基线横断面数据让我有点惊讶,但也不是特别惊讶,因为(a)演示中的数据留下了很多问题,我希望论文能够解决这些问题,(b)这是一个非常小的横断面分析,有很多局限性和潜在问题。 话虽如此,我是否认为 LMHR 的动脉粥样硬化斑块进展不会比对照组更快?是的,绝对如此,我甚至有几个假设可以解释为什么会这样。是的,这些假设确实包括关键脂蛋白的组成差异,无论是脂质还是——也许更重要的是——蛋白质载量。因为当我在视频中只谈论 apo B、apo (a) 和 apo A 时,这些脂蛋白确实携带着许多其他蛋白质,其中一些蛋白质与动脉粥样硬化有关。我还假设 LMHR 的 LDL 胆固醇在餐后会下降,而且比吃混合饮食的人下降得多。部分由于这个原因,我认为可以合理地假设 LMHR 全天的平均 apo B 浓度与对照组相比并没有高出那么多。 因此,是的,有很多潜在原因导致 LMHR 的 ASCVD 风险可能与目前的假设有很大不同。但是,重要的是要记住,所有这些都只是目前的假设,鉴于从所有其他人群中获得的大量数据,最好的估计应该是动脉粥样硬化斑块在 LMHR 中的进展速度将比在对照组中更快。此外,如果发现 LMHR 没有经历 ASCVD 进展,那么他们将是有史以来第一个证明 LDL 胆固醇大幅升高与 ASCVD 进展脱钩的人群。对于 LMHR 来说,这将是一个相当大的问题,但对于这个领域也是如此。 祝好, 马里奥 - 4c621fda7bd799be9e16332714e0f7e2保罗 说: 2023 年 12 月 20 日上午 7:20 Mario,请观看 Paul Mason 博士的短片“心脏病真正原因的硬科学”,并发表评论。他提供了有力的证据来反驳脂质假说,并指出凝血是风险因素之一,而您似乎并未将其列入 CVD 独立风险因素列表中。 - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2024 年 1 月 13 日下午 2:06 嗨,保罗, 我知道有人声称,血液凝结而非载脂蛋白 B 的滞留是导致动脉粥样硬化形成的原因。这是一个有趣的假设,有一些相关数据支持这一想法。例如,动脉粥样硬化斑块确实含有来自血小板和红细胞的物质,而脂质模型无法很好地解释这些物质是如何到达那里的。尽管如此,支持血栓是唯一原因这一观点的数据基本上是不存在的。如果有的话,目前的数据充其量只能支持循环中的微凝块可能在动脉粥样硬化形成中发挥作用的假设。在我看来,这远非明确,我也不明白为什么血液凝结假说的支持者将其视为反对血脂在 ASCVD 中发挥作用的证据,因为有更多、更强有力的证据来证明这一点。 我正在关注这个领域,并对进一步的证据感兴趣,但我在现有的科学文献中没有看到任何内容让我感到携带 app B 的脂蛋白不重要。 祝好, 马里奥 - 036c66cdc1f60729a9abd1dfdd4d244c詹姆斯·哈德森 说道: 2023 年 12 月 20 日晚上 11:31 关于:“ASCVD 是一种多因素疾病”。我对另外两个已知与 ASCVD 密切相关或可能导致 ASCVD 的因素感兴趣,但我很少在过去的大多数博客和 YouTube 上看到被提及。第一个是尿酸的作用。自 Perlmutter 博士的著作《Drop Acid》出版以来,这在去年受到了更多的关注。 第二个比尿酸升高少见得多。铁过载,主要由遗传性血色素沉着症引起。许多研究表明,会导致全身炎症,包括心脏和心血管问题。幸运的是,一旦发现自己患有这种疾病,就很容易控制。 我想听听您对尿酸和 ASCVD 科学的看法。谢谢! - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2023 年 12 月 21 日上午 12:17 嗨,詹姆斯, 好问题。 铁过载显然是 ASCVD 风险因素,但这是一种遗传疾病,有许多都被视为遗传疾病。在这篇博文中,我介绍了那些广泛适用于普通人群的风险因素。尽管在男性中,人们当然可以争论铁摄入量超过正常水平是否会带来一定风险。 尿酸是众多新兴 ASCVD 风险因素之一,我认为,我们慢慢地有了足够的数据来考虑,并了解与其他 ASCVD 风险因素的关系(这对于确定风险因素是否独立于其他因素很重要)。我可能会在不久的将来制作一个关于这个的单独视频,因为其他人也要求这样做。 干杯 马里奥 - d71ac269f900e97e74360deb117ea52a大卫·巴恩斯 说道: 2023 年 12 月 24 日上午 12:58 嗨,Mario, 有关于以下问题的研究吗? 如果存在“严重”动脉钙化,服用他汀类药物是否有任何已证实的益处?这听起来就像“马儿跑了才关上马厩的门”。从我在网上找到的信息来看,钙化斑块被认为是“稳定的”,风险小于热/软斑块。 目前的口号似乎是,任何钙化分数高的人都应该立即服用高剂量的他汀类药物。 似乎更合适的做法是首先尽可能改变生活方式,以解决您精彩视频中涵盖的风险因素。 目的是阻止软斑块进一步形成。如果相关脂质标志物在生活方式改变后仍然很高,则可能需要服用他汀类药物(从低剂量开始)。 似乎对已经钙化的斑块无能为力(尽管目前的热门话题是,补充维生素 K2 可能会做到这一点)。 如果您在之前的视频中涵盖了这些内容,能否提供相关链接。 您可以在未来的视频中讨论动脉斑块的各种状态及其后果吗? - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2023 年 12 月 24 日下午 1:49 这个问题问得非常好,但问题又很复杂。请允许我在这里给您一个简短的回答:一般来说,如果有人发生过 ASCVD 事件,那么大家的共识是始终开他汀类药物以尽可能降低载脂蛋白 B,而且因为他汀类药物的一些其他非脂质相关作用可能有助于预防另一起事件。对于未发生过 ASCVD 事件的钙化斑块患者,情况不太清楚,但我仍然认为大多数预防心脏病专家会使用“以上所有”方法,尽可能降低所有风险因素,以防止出现更多斑块和现有斑块恶化。总的来说,我认为这是有证据支持的,尽管一般来说,他汀类药物在一级预防(在任何 ASCVD 事件之前)中的使用没有在二级预防中得到充分的数据支持。 干杯 马里奥 - d71ac269f900e97e74360deb117ea52a大卫·巴恩斯 说道: 2023 年 12 月 26 日凌晨 2:02 非常感谢您的,希望您将来能制作一个关于这个主题的视频。我看到有许多外科手术可用于物理去除动脉斑块,但我不确定这些手术是否适用于冠状动脉。动画看起来有点吓人,似乎钻出/磨损了动脉沉积物。一个过程似乎是用一根电线“消灭”钙沉积物。我不记得他们是否使用电流或某种冲击波来分解钙颗粒。这一切都有点令人担忧,有什么评论吗? - 6058f28f44e8040e8b5e028199411672Karl BIederstadt 说: 2023 年 12 月 30 日上午 10:20 你好,Kratz 医生, 在观看了您在 Ford Brewer 医生的网络广播中的演讲后,我了解到您的工作,并立即为您的纪律和风度产生了共鸣。一年前,冠状动脉 CT 扫描的 Agatston 评分为 880(总分),左前降支为 660。我以前的全科医生让我在过去 15 年里服用 10 毫克瑞舒伐他汀,但我对他对扫描结果对我的冠状血管健康状况的暗示的解释并不满意。经过网上搜索,我找到了 Brewer 医生的 Prevmed 网站和 YouTube 频道。我相信 Prevmed 和 Brewer 医生在预防 ASCVD 方面大有可为,并想采用他的方法,使用低剂量的他汀类药物来减少内皮炎症和软斑块的进展。我本来准备面对我的新全科医生和她将我的瑞舒伐他汀增加到 20 毫克的建议,但考虑了您的评论后,我选择接受我的新全科医生的建议。我认为这是一个明智的选择,因为我没有经历过瑞舒伐他汀的任何负面副作用。请继续努力。 - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2024 年 1 月 3 日下午 2:05 谢谢。 - 7986d4e02afa87cffa43fca45ddd2e13克里斯 说: 2024 年 1 月 12 日下午 3:31 感谢马里奥开设了专注于事实的频道。 我理解任何都是一般性的,而不是专门针对我的医疗建议。 我是一名 55 岁的男性,CAC 评分为 486。除了家族病史和男性身份外,我没有任何 ASCVD 的标准风险因素。无高血压、无吸烟、无饮酒、无肥胖、无糖尿病、无高胆固醇、无肾病。 自 2006 年以来,平均 LDL-C 为 76,HDL 为 41,总计 131,甘油三酯为 72。 我的目标是确定 ASCVD 的根本原因(也许这是不可能的),这样我才有最大的机会限制其进展。我的医生立即给我开了 40 毫克阿托伐他汀,我服用了几个月,然后因为肌肉问题停药。这使我的 LDL 降至 45,ApoB 降至 31。我相信这些结果表明,即使在开始服用他汀类药物之前,我的 ApoB 也不高。服用他汀类药物时,C 反应蛋白为 0.31。我认为这表明我没有慢性炎症。 在 2006 年之前,我体重超标,很可能处于糖尿病前期,这种情况持续了至少 5 年甚至更久。从 2006 年开始,我减掉了 30 多磅,从那时起一直保持在这个水平或以下。自 2006 年以来,BMI 一直低于 27,大多数时候都低于 26。从那时起,血糖和 A1C 都处于正常范围内。从 2006 年开始,我对糖和热量摄入量进行了大幅度的调整,因此看来我的饮食在过去 17 年里并不是导致 ASCVD 的主要因素。 1. 对于具有此类特征的个体,研究对于 ASCVD 的根本原因有何看法? 2. 我的 CAC 分数是否可能长期保持较高水平而我却根本不知道? 3. 对于 CAC 评分高但 LDL 或 ApoB 不高的患者,研究如何评价他汀类药物的疗效? 我的研究表明,低剂量的高效他汀类药物或低效他汀类药物(如普伐他汀)可能有利于获得他汀类药物的非降脂作用。 亲切的, 克里斯 - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2024 年 1 月 13 日凌晨 1:02 嗨,克里斯, 我想,你的情况有点令人沮丧。如果是我,我会进一步研究以下几点: – 测量我的 Lp(a)浓度。即使您的 LDL 没有升高,Lp(a) 也可能很高,并可能使您进入高风险类别。Lp(a) 被认为是高度遗传的,可以解释家族史。虽然目前没有批准可以有效降低 Lp(a) 的药物,但有几种药物正在处于终末期临床试验中,因此了解这一点很重要。 – 另一种可能导致 ASCVD 的遗传异常。在男性身上立即想到的是血色素沉着症(铁储存疾病)或威尔逊氏病(铜储存疾病)或类似疾病。 – 慢性炎症,例如自身免疫性疾病。 我还会密切关注血压(在家定期测量)和血糖水平(也许佩戴 CGM 几周,看看是否出现频繁的飙升模式),并确定 HOMA-IR(参见我关于测量胰岛素抵抗的视频/博客文章)。 ASCVD 可能是由于您的遗传风险 + 几年来超重、胰岛素抵抗和糖尿病前期而导致的,但仅凭这一点,我就觉得不太可能,因为听起来这些参数都没有真正糟糕过?没有明显的糖尿病,BMI 没有 > 30?您知道 2006 年之前的 LDL-chol 吗?但是,您仍然有可能在一段时间内患有冠状动脉斑块和可能的钙化斑块,而您却不知道。目前还无法确定。 我个人的观点是 (a) 找出病因,(b) 尽量减少可能促进病情进展的所有因素。这意味着要服用降脂药物,但我不会仅仅忍受副作用,而是尝试不同的副作用或不同的剂量。我同意,即使在 LDL-chol/apo B 水平相当低的情况下,他汀类药物也可能有益,部分原因是它可以进一步降低 LDL-chol/apo B(从 76 毫克/分升到 45 毫克/分升是有意义的),部分原因是它的其他作用(稳定斑块、抗炎作用)。 我知道您明白,这不是医疗建议,我强烈建议您与医生讨论这些要点。 希望这对您有帮助。祝您好运! 祝您好运, 马里奥 - 7986d4e02afa87cffa43fca45ddd2e13克里斯 说: 2024 年 1 月 13 日凌晨 3:01 我确实检查过我的 Lp(a),结果为 < 10 nmol/L,所以还好。遗憾的是,我没有 2006 年之前的胆固醇数据。 我的最高 BMI 约为 30,但维持的时间不超过一两年。与胆固醇数据一样,我没有 2006 年之前的其他医疗数据,但我 2006 年的基线空腹血糖为 130。当时我的体重最高,所以我怀疑我的体重从未超过这个数字。 我目前正在与一位功能医学医生合作,希望找出病因,但我越来越怀疑自己是否真的能找到病因。我现在的心脏病专家对这项研究不感兴趣,所以我才去找了一位功能医学医生。我知道功能医学医生在传统医学界名声不好。我正在看的医生是一位获得认证的内科医生,从事内科工作已有 20 年,所以希望我能得到很好的照顾。她对我的血液测试的解释是,我目前没有胰岛素抵抗。我的胰岛素和血糖血液测试的 HOMA-IR 为 1.4。 我会考虑使用 CGM 并监测我的血压。我没有您提到的两种遗传异常的症状。我的湿疹非常轻微,这可能表明我患有某种自身免疫或炎症疾病。也许除了 C 反应蛋白之外还有其他测试可以识别慢性炎症? 非常感谢您提供如此周到的。 克里斯 - d9c85c066cf0b227af4b6dd7d2b75311Jeff C. 说: 2024 年 1 月 20 日下午 2:52 很棒的文章,将我一直不太清楚的血脂的许多细节联系在一起。用通俗易懂的语言写得很好,谢谢。 一直困扰我的一个方面是独立风险因素的概念,因为似乎是一个有缺陷的前提。代谢综合征表现为一组症状(肥胖、低 HDL、高甘油三酯、高 A1c 等),许多相关疾病也是如此。因此,单一指标的相关性总是非常弱,如果有的话,因为很少在没有其他指标的情况下出现。总体模式才是最重要的,这就是为什么生酮饮食对普通人的风险状况有显著影响,而仅仅让他服用他汀类药物最多只能起到微不足道的作用。 Nick 和 Dave 对 LMHR 的研究似乎证实了这一点。此外,为什么他们描述的完全相同的机制不适用于生酮饮食的普通人乔先生?使用(在我看来值得怀疑的)评分方法,他的风险在生酮饮食中从 39.4% 下降到 14.5%。哪里有证据表明额外降低 LDL(也许使用他汀类药物)会降低他的风险?只有当人们认为这些成分单独来看非常重要时才会这样做,但事实似乎并非如此。 在我看来,这种想法很大程度上是由药物开发推动的,药物开发使用代理终点(例如降低 LDL)而不是测量更少的死亡人数。理论上,这是有道理的,因为测量脂质比在足够长的时间内招募足够多的参与者以积累足够多的尸体更容易。但问题是,代理终点很容易因无能或公然恶意而被滥用。过度关注单一参数的重磅药物开发充其量只是一叶障目。 - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2024 年 2 月 8 日下午 1:53 嗨,杰夫, 感谢您深思熟虑的评论。 “独立”风险因素的概念主要基于风险生物标志物是否在统计上与 ASCVD 独立相关,即在调整了所有其他已知风险因素之后。话虽如此,我同意你的观点,很难证明任何生物标志物本身在病理生理学上完全独立于所有其他因素。 话虽如此,我认为使用现有数据进行风险评估是目前能做到的最好的事情。如果得到新数据表明确实存在效果修正,例如,对于某些人来说,LDL大幅升高不再与 ASCVD 有关,那么就可以更新风险预测模型。目前,不存在这样的效果修正,我认为根据目前相当于假设的内容告诉人们忽略过高的 LDL是不负责任的。需要考虑的是,在所有脂质研究中,没有发现任何 LDL与 ASCVD 之间存在脱节的情况(即真正的效果修正)。 干杯 马里奥 - 8e9bd4401a41e5419f20bdd01f59e7fe让-雅克·帕斯卡·桑塔雷利 说: 2024 年 1 月 21 日下午 1:31 您好,再次感谢您非常清晰的解释。 除了 LDL、apoB 和脂蛋白 (a) 水平外,动脉超声检查是否也能通过量化沉积物的存在和数量来提供信息或确认风险水平,尤其是从动态角度(例如每 3-5 年检测一次)? 您提到了风险因素,并强调了肉类消费:是什么原因导致肉类会升高血液中的 LDL/apoB 水平?这是否因所食用肉类的类型和质量而异(例如,鸡胸肉等瘦肉,或来自以草为食的大规模养殖场的肉类与以大豆/玉米为食的肉类)? 提前感谢您的, 让·雅克 - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2024 年 2 月 8 日下午 1:56 你好,Jean-Jacques, 大部分都是肥肉,因为其中富含长链饱和脂肪酸,与不饱和脂肪酸相比,饱和脂肪酸会升高 LDL 胆固醇。这不会产生很大影响,而且对 ASCVD 风险的影响有点不确定,我将在未来的视频中讨论。 干杯 马里奥 - 7156075e2f18e93edf48b1140cea4f64法比安 说: 2024 年 1 月 21 日下午 6:50 嗨,Mario,谢谢你的文章,非常有用。 我知道,你提到的各种因素都必须考虑到 ASCVD 的总体风险。 如果我只是担心 apoB 水平略有升高(93mg/dl),我可以采取什么非药物方式来降低它(食物类型、补充剂等)? 一点背景信息,33 岁,身体状况良好,心情愉快,经常锻炼。(TG:54mg/dl,HDL:55mg/dl,LDL:126mg/dl) 谢谢 - 7312d72da6f04845de86ba4a293874d0迈克尔 说: 2024 年 1 月 26 日下午 2:48 您好, 93mg/dl 在哪个指标下略微升高(谁的建议)? - 7156075e2f18e93edf48b1140cea4f64法比安 说: 2024 年 2 月 3 日上午 9:15 嗨,Michael,ApoB 为 93mg/dl。从我读到的内容来看,LDL 颗粒数量与 ASCVD 之间的联系非常明显。体内的颗粒越多,在较长时间内,患 ASCVD 的风险就越大。 为什么我认为它略有升高,我依赖于 Framingham 的研究(Contois、John H 等人 2009),所以我处于人口的 45 百分位数。 我希望处于人口的 20 百分位数(78mg/dl ApoB)或更低。 - 44c48b82b5e95b04baf5443ab6cbc25b马丁·辛克莱 说道: 2024 年 1 月 23 日下午 10:16 显而易见的是,目前还没有提出任何方法来远程解释高 LDL 或 ApoB 确实如何(即机制)导致动脉粥样硬化…但对于动脉粥样硬化如何发生,有非常合理的机制,而 LDL 并不是病因(例如 Kendrick 博士的血栓假说,或者实际上只是血糖/胰岛素导致的糖萼降解)…如果没有任何机制,心血管疾病中存在的高 LDL/ApoB 很可能是一个指示性生物标志物…火灾现场的消防员而不是纵火犯。 - 7312d72da6f04845de86ba4a293874d0迈克尔 说: 2024 年 1 月 26 日上午 9:19 你好,马里奥, 论文《载脂蛋白 B 作为心血管风险标志物优于低密度脂蛋白胆固醇和非高密度脂蛋白胆固醇的生理基础》 你可以找到以下语句: “从肝脏输出的 VLDL颗粒中的胆固醇,又以 VLDL 或 LDL 颗粒的形式返回,这经历了什么生理过程?这 只是胆固醇的无用循环,还是胆固醇和 CE 是形成 VLDL颗粒的必要元素?或者,至少在某些情况下,VLDL 颗粒也会从肝脏输出过量的胆固醇?这些问题目前尚无答案。” 这是真的吗?在 2024 年,我们仍然不知道为什么胆固醇会在血液中的脂蛋白中循环? 在同一篇论文中提到,外周细胞不会使用或吸收脂蛋白中的胆固醇! 令人困惑。 问候迈克尔 - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2024 年 2 月 8 日下午 2:35 好问题。所有细胞都可以制造自己的胆固醇,因此确实不需要从循环中吸收。然而,几乎所有组织都表达与载脂蛋白 B 结合的 LDL 受体分子,可以从循环中去除 LDL 颗粒,因此这表明细胞确实在某种程度上从循环的载脂蛋白中获取部分胆固醇。不过,据估计,大约 70% 左右的所有 LDL 颗粒都是由肝脏从血液中去除的,因此考虑到 LDL 最初是由肝细胞分泌的(作为 VLDL),这部分似乎是一个无用循环。 我最好的猜测是肝脏需要使用胆固醇作为包装材料来组装 VLDL 颗粒。将 TG 输出到 VLDL 颗粒中只是肝脏清除甘油三酯的两种方式之一。我在这里谈到了这一点: <https://nourishedbyscience.com/insulin-resistance-syndrome/> 干杯 马里奥 - 7ca8969e9cadeb124d0bfcd16d8f610e艾略特 说: 2024 年 2 月 21 日下午 4:26 我对此视频有一些疑问。我只会列出要点,而且我懒得查找许多参考资料。 – 您似乎忽略了那些没有奏效的降低胆固醇或 LDL 的方法。烟酸可降低 LDL 和甘油三酯并提高 HDL。胆汁酸螯合剂已被尝试但失败了。CETP 抑制剂使血液检查结果看起来不错,但也未显示出任何益处。 – 我还没有看到任何关于 PCSK9 抑制剂单独使用的研究显示其有益。有些研究将它们与他汀类药物一起服用,有些研究将它们单独服用并降低了替代标志物。 – 有没有关于普通人群的数据表明降低总胆固醇/LDL/ApoB 有任何好处。服用他汀类药物的人很多,心血管疾病应该有所减少,但据我所知,心血管疾病发病率却在增加。 – 您提到了 LP(a),但我不记得您说过它通常与 LDL 一起计算。也许我没注意到。 您没有提到他汀类药物可能具有的多效性。最早显示他汀类药物有益的研究之一(见上面评论)得出的结论是“我们降低了胆固醇,心脏病发作的几率 [几乎没有显著] 降低了。”不,他们服用了他汀类药物,得到了这样的结果。 - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2024 年 2 月 22 日下午 12:51 艾略特, 恕我直言,过去 30 多年来,我在这个领域研究了 1,000 多篇论文,这里引用了 23 篇关键论文。你通过发表声明来反驳这一点,但没有提供任何证据。不知道你希望我如何回应。在这个主题的浩瀚文献中很容易找到一些异常值。因为当然也有一些例外,但你真的认为从根本上质疑这里提出的内容就足够了吗? 而且更具体地说,如果您是我,您是否认为这些不一致的数据点足以告诉我的所有读者忽略他们的血清脂质? 祝好, 马里奥 - 2a53b9fc78854f35d9d0a80e2ab70420泰·比尔 说道: 2024 年 2 月 24 日下午 3:49 非常感谢,Mario。我做了一个自我实验,看看我是否可以通过改变饮食来降低我的 apoB(目前为 103 mg/dL)。我戒掉了鸡蛋,限制了饱和脂肪和其他胆固醇来源,并吃了大量的豆类,持续了两个月。这对我的 apoB 没有影响,并使我的甘油三酯从 79 mg/dL 增加到 101 mg/dL。鉴于可行的饮食变化似乎对我的 apoB 没有影响,并且我的 Lp(a) 为 126 nmol/L,你会建议我和医生谈谈药物疗法吗?我不知道家族有 CVD 病史。我的医生说一切都很好,不用担心。但根据您的建议,我认为通过药物疗法降低我的 apoB 可能是值得的。 - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2024 年 2 月 24 日下午 4:11 嗨,Ty, 我知道您明白我无法在这里提供医疗建议,因此下面我建议的所有内容都只是一些值得思考的内容,需要与医生进一步讨论。 您的情况属于边缘病例。126 nmol/L 的 Lp(a) 相当于 50 mg/dL,这表明您的 Lp(a) 相关风险升高。这意味着您的其他风险因素最好得到更严格的控制。如果有人没任何其他 ASCVD 风险因素,那 Apo B 本身为 103 mg/dL,大多数医生可能不会对其进行治疗,但是随着 Lp(a) 升高,一些心脏病专家可能会考虑使用低剂量的降脂药物,因为饮食改变无法成功降低 Apo B。这里要理解的一件事是,绝对 ASCVD 风险在不久的将来(例如未来 10 年)可能很低,因此人们考虑在此阶段降低 Apo B 的主要原因是降低 20 年甚至 30 年后发生 ASCVD 事件的风险,以降低累积的终生暴露。好的,现在是时候考虑一下,到您 60、70 或 80 岁时,您的一生中 Apo B 的累积曲线下面积会是多少。我认为,只有当降脂药物耐受性良好(没有肌肉相关副作用,没有增加胰岛素抵抗和葡萄糖不耐受)时,开始药物治疗的相对较小的短期益处才有意义。这就是我对此的看法,并且可能会与预防心脏病专家讨论这些观点,以仔细权衡益处与潜在风险。 祝一切顺利, 马里奥 - 7d971f9c5c39e6b3c7f588384cc24133克里斯 说: 2024 年 5 月 6 日下午 12:38 就血液测试而言,PLAC 测试怎么样? - 7209fe756c543914dcc5b6dc9eafd49b马里奥·克拉茨 说道: 2024 年 5 月 6 日下午 11:12 克里斯, 您可以在此处阅读相关内容: <https://www.aafp.org/pubs/afp/issues/2020/0101/p44.html> 我猜想,保险可能不涵盖这项测量,而且我个人不会为此付费。 干杯 马里奥 Edit:2024.09.28 ====== 即使没有其他心血管危险因素,高脂蛋白(a)也需要干预 ====== 一项新研究表明,无论是否存在心血管疾病的标准可改变风险因素,这一经常被忽视的指标与心脏病发作密切相关 Kathryn Birkenbach、Tom Dayspring、Peter Attia 2024 年 6 月 1 日
 风险
—-
在考虑如何评估和降低慢性病风险时,人们往往倾向于只关注可改变的风险因素。例如,我们可以戒烟、减掉多余的脂肪或服用药物来降低升高的血压或胆固醇水平。但在心血管疾病 (CVD) 的风险评估和管理策略方面,一个不可改变的因素绝不能忽视:脂蛋白 (a),通常称为 Lp(a)。
正如Benoit Arsenault 博士在播客中解释的那样,Lp(a) 升高是 CVD 最重要的遗传风险因素,也是最常见的遗传风险因素,但我们目前缺乏任何简单的治疗方法。事实上,由于没有降低高 Lp(a) 的方法,许多医生甚至懒得测试这个变量。但一项新研究的结果强调了 Lp(a) 对 CVD 风险评估的重要性,以及尽管缺乏改变 Lp(a) 水平的方法,但这一指标仍可能对风险管理决策产生重大影响。
===== 研究设计和队列 =====
Shiyovich 等人的回顾性研究调查了 Lp(a) 与急性心肌梗死 (MI,也称为心脏病发作) 之间的关联,以及这种关联与心脏病的标准可改变风险因素 (SMuRF) 之间的关系。¹ (我承认,对我来说,如果不去想“SMuRF”这个词,就有点难以坚持下去。)研究人员利用了2000年 1 月至 2019 年 7 月期间在波士顿地区接受过常规 Lp(a) 检测的 6,238 名成年人(平均年龄:54 岁;45% 为女性)的数据(来自麻省总医院布莱根 Lp(a) 登记处)。患有严重肾功能障碍、癌症或先前已知的动脉粥样硬化性心血管疾病的个体的数据被排除在研究之外。对参与者进行了中位 8.8 年的随访,以评估致命或非致命性 MI 的发病率。
如果参与者的 Lp(a) 水平超过第 90 百分位(基于已建立的全人群参考范围),则被归类为“高 Lp(a)”;如果参与者的 Lp(a) 水平低于第 50 百分位,则被归类为“低 Lp(a)”,高截断值和低截断值分别对应 >168 nmol/L 和 <19 nmol/L。总体而言,参与者的 Lp(a) 水平略低于一般人群,58% 的参与者符合低 Lp(a) 的定义,7% 的参与者符合高 Lp(a) 的定义。
SMURF 定义为高血压、吸烟、糖尿病或非 Lp(a) 血脂异常,非 Lp(a) 血脂异常定义为:1) 总胆固醇 ≥240 mg/dL;(2) LDL 胆固醇 ≥160 mg/dL;(3) HDL 胆固醇(男性)<40 mg/dL 或女性<50 mg/dL;或 (5) 总甘油三酯≥175 mg/dL。值得注意的是,相当大比例的参与者(23.7%)没有 SMuRF,而 17.8% 至少有三个。随着 SMuRF 数量的增加,高Lp(a) 的发生率也略有增加,而低Lp(a)的发生率则下降。
===== SMuRF 和高 Lp(a) 会增加心脏病发作风险 =====
作者报告称,在随访期间共有 234 名参与者 (3.75%) 经历了急性 MI。正如预期的那样,在整个队列中,SMuRF 数量越多,发生 MI 的风险就越高,与没有 SMuRF 相比,两个 SMuRF 对应的风险增加三倍 (HR=3.05;95% CI:1.93-4.83;P <0.001),≥3 个 SMuRF 对应的风险增加 6.5 倍 (HR=6.51;95% CI:4.18-10.16;P <0.001)。当对低 Lp(a) 和高 Lp(a) 亚组进行独立分析时,这种趋势仍然存在。这并不令人惊讶。
但该研究最重要的发现是,在所有数量的 SMuRF 中,高 Lp(a) 与 MI 风险的相关性高于低 Lp(a)(见下图),这表明*无论是否存在其他风险因素,*升高的 Lp(a) 都是心脏病发作的主要风险因素。事实上,Shiyovich 等人报告称,高 Lp(a) 患者的风险是低 Lp(a) 患者的 3 倍多(HR=3.19;95% CI:2.20-4.65;P <0.001),因此高 Lp(a) 带来的风险增加相当于拥有两个 SMuRF 相关的风险增加。
风险
—-
在考虑如何评估和降低慢性病风险时,人们往往倾向于只关注可改变的风险因素。例如,我们可以戒烟、减掉多余的脂肪或服用药物来降低升高的血压或胆固醇水平。但在心血管疾病 (CVD) 的风险评估和管理策略方面,一个不可改变的因素绝不能忽视:脂蛋白 (a),通常称为 Lp(a)。
正如Benoit Arsenault 博士在播客中解释的那样,Lp(a) 升高是 CVD 最重要的遗传风险因素,也是最常见的遗传风险因素,但我们目前缺乏任何简单的治疗方法。事实上,由于没有降低高 Lp(a) 的方法,许多医生甚至懒得测试这个变量。但一项新研究的结果强调了 Lp(a) 对 CVD 风险评估的重要性,以及尽管缺乏改变 Lp(a) 水平的方法,但这一指标仍可能对风险管理决策产生重大影响。
===== 研究设计和队列 =====
Shiyovich 等人的回顾性研究调查了 Lp(a) 与急性心肌梗死 (MI,也称为心脏病发作) 之间的关联,以及这种关联与心脏病的标准可改变风险因素 (SMuRF) 之间的关系。¹ (我承认,对我来说,如果不去想“SMuRF”这个词,就有点难以坚持下去。)研究人员利用了2000年 1 月至 2019 年 7 月期间在波士顿地区接受过常规 Lp(a) 检测的 6,238 名成年人(平均年龄:54 岁;45% 为女性)的数据(来自麻省总医院布莱根 Lp(a) 登记处)。患有严重肾功能障碍、癌症或先前已知的动脉粥样硬化性心血管疾病的个体的数据被排除在研究之外。对参与者进行了中位 8.8 年的随访,以评估致命或非致命性 MI 的发病率。
如果参与者的 Lp(a) 水平超过第 90 百分位(基于已建立的全人群参考范围),则被归类为“高 Lp(a)”;如果参与者的 Lp(a) 水平低于第 50 百分位,则被归类为“低 Lp(a)”,高截断值和低截断值分别对应 >168 nmol/L 和 <19 nmol/L。总体而言,参与者的 Lp(a) 水平略低于一般人群,58% 的参与者符合低 Lp(a) 的定义,7% 的参与者符合高 Lp(a) 的定义。
SMURF 定义为高血压、吸烟、糖尿病或非 Lp(a) 血脂异常,非 Lp(a) 血脂异常定义为:1) 总胆固醇 ≥240 mg/dL;(2) LDL 胆固醇 ≥160 mg/dL;(3) HDL 胆固醇(男性)<40 mg/dL 或女性<50 mg/dL;或 (5) 总甘油三酯≥175 mg/dL。值得注意的是,相当大比例的参与者(23.7%)没有 SMuRF,而 17.8% 至少有三个。随着 SMuRF 数量的增加,高Lp(a) 的发生率也略有增加,而低Lp(a)的发生率则下降。
===== SMuRF 和高 Lp(a) 会增加心脏病发作风险 =====
作者报告称,在随访期间共有 234 名参与者 (3.75%) 经历了急性 MI。正如预期的那样,在整个队列中,SMuRF 数量越多,发生 MI 的风险就越高,与没有 SMuRF 相比,两个 SMuRF 对应的风险增加三倍 (HR=3.05;95% CI:1.93-4.83;P <0.001),≥3 个 SMuRF 对应的风险增加 6.5 倍 (HR=6.51;95% CI:4.18-10.16;P <0.001)。当对低 Lp(a) 和高 Lp(a) 亚组进行独立分析时,这种趋势仍然存在。这并不令人惊讶。
但该研究最重要的发现是,在所有数量的 SMuRF 中,高 Lp(a) 与 MI 风险的相关性高于低 Lp(a)(见下图),这表明*无论是否存在其他风险因素,*升高的 Lp(a) 都是心脏病发作的主要风险因素。事实上,Shiyovich 等人报告称,高 Lp(a) 患者的风险是低 Lp(a) 患者的 3 倍多(HR=3.19;95% CI:2.20-4.65;P <0.001),因此高 Lp(a) 带来的风险增加相当于拥有两个 SMuRF 相关的风险增加。
 图:**按标准可修改风险因素 (SMuRF) 数量和低 Lp(a) 与高 Lp(a) 定义的亚组急性心肌梗死发病率。误差线表示 95% 置信区间。绿色箭头显示高 Lp(a) 带来的超额风险与两个 SMuRF 相关的超额风险相当。改编自 Shiyovich et al. 2024。
图:**按标准可修改风险因素 (SMuRF) 数量和低 Lp(a) 与高 Lp(a) 定义的亚组急性心肌梗死发病率。误差线表示 95% 置信区间。绿色箭头显示高 Lp(a) 带来的超额风险与两个 SMuRF 相关的超额风险相当。改编自 Shiyovich et al. 2024。
这对心血管疾病风险管理决策有何影响?
这些结果表明,无论患者是否具有其他风险因素,高 Lp(a) 都是 CVD 的主要风险因素,因此,应始终积极治疗高 Lp(a) 患者。但正如我们之前提到的,我们缺乏降低 Lp(a) 水平的药物或行为选择。(一些医生使用 PCSK9 抑制剂来降低 Lp(a) 约 25%,但结果变化很大,并且这种水平的 Lp(a) 降低可能不足以显着降低 CVD 风险。)因此,尽管这项研究证实了 Lp(a) 升高与心血管事件风险之间的密切关联,但这些知识有任何实际用途吗?如果您无法采取任何措施降低 Lp(a),那么发现自己患有高 Lp(a) 是否值得?
绝对如此。虽然我们可能无法降低 Lp(a) 本身,但我们可以通过治疗其他CVD 风险因素来降低总体 CVD风险。因此,发现特定患者 Lp(a) 水平高可以作为高血压、糖尿病,尤其是 apoB 水平升高(或不太准确地说是 LDL-C)的征兆,应比其他情况下更积极地管理,以抵消Lp(a) 带来的风险。
小结
Shiyovich 等人的研究强调,高 Lp(a) 是动脉粥样硬化性心血管疾病的主要遗传风险因素,即使在没有其他危险信号的人中也是如此,但许多 Lp(a) 水平高的人却没有意识到这一点,因为这一指标经常被忽视和测试不足。幸运的是,人们越来越意识到 Lp(a) 对 CVD 风险的重要性;越来越多的医疗机构对这一变量进行测试,一些公司甚至开始向消费者销售直接面向消费者的家用 Lp(a) 检测试剂盒。但最终,仅仅知道自己的 Lp(a) 水平高只是第一步。为了降低 CVD 事件的风险,必须利用这些信息来激励人们采取更积极的方法应对其他可改变的风险因素。
参考
1. Shiyovich A、Berman AN、Besser SA 等。脂蛋白 (a) 和标准可改变心血管风险因素与心肌梗死发生率的关系:麻省总医院 Brigham Lp(a) 登记处。J Am Heart Assoc。2024;13(10):e034493。doi:10.1161/JAHA.123.034493
https://peterattiamd.com/high-lpa-risk-factors/
Edit:2024.09.28












